题目内容
【题目】以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如下所示。
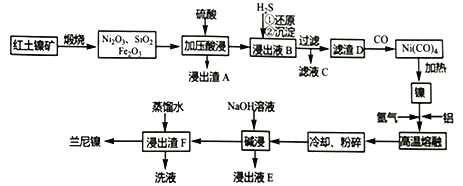
(1)形成Ni(CO)4时碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为___________。
(2)Ni2O3有强氧化性,加压酸浸时有气体产生且镍被还原为Ni2+,则产生的气体为______(填化学式)。
(3)滤渣D为单质镍、硫的混合物,请写出向浸出液B中通入H2S气体时所有反应的离子方程式:__________________________,_________________________。
(4)已知:3Fe2++2[Fe(CN)6]3-==Fe3[Fe(CN)6]2↓(蓝色沉淀);下列可以用于检验滤液C中金属阳离子的试剂有____________(填标号)
a.KSCN溶液 b.K3[Fe(CN)6] c.K4[Fe(CN)6] d.苯酚
(5)仿照下面示例,设计从浸出液E回收氧化铝的流程:浸出液E_______________。
(示例:CuO![]() Cu2+
Cu2+![]() Cu)
Cu)
【答案】0 O2 H2S+2Fe3+==2Fe2++2H++S↓ H2S+Ni2+==Ni↓+2H++S↓ b ![]() Al(OH)3
Al(OH)3![]() Al2O3
Al2O3
【解析】
红土镍矿煅烧NiS、FeS生成Ni2O3、Fe2O3,加压酸浸时,Ni2O3被还原为Ni2+,Fe2O3溶解生成Fe3+,浸出液B的主要成分是NiSO4和Fe2(SO4)3,滤渣A为SiO2;通入H2S气体时,Fe3+、Ni2+发生还原反应,滤渣D为单质镍、硫的混合物,滤液C为FeSO4和H2SO4;单质镍、硫的混合物中通入CO,镍与CO生成Ni(CO)4;Ni(CO)4加热分解生成Ni;在氢气气氛中,Ni和Al高温熔融冷却得到Ni、Al合金;Ni、Al合金中加入氢氧化钠溶液,铝与氢氧化钠溶液生成偏铝酸钠,放出氢气,浸出液E为偏铝酸钠溶液,滤渣F为Ni。
(1)在Ni(CO)4中,碳元素的化合价与CO相同,为+2价,故Ni的化合价为0,故答案为0;
(2)已知Ni2O3有强氧化性,加压酸浸时有气体产生且镍被还原为Ni2+,说明Ni元素被还原,则反应只能是O元素被氧化为O2,故答案为:O2;
(3)滤渣D为单质镍、硫的混合物,说明通入H2S时,Fe3+、Ni2+发生还原反应,反应的离子方程式为:H2S+2Fe3+=2Fe2++2H++S↓;H2S+Ni2+=Ni↓+2H++S↓;
(4) 通入H2S时,Fe3+、Ni2+发生还原反应,滤渣D为单质镍、硫的混合物,滤液C中含有Fe2+离子和H+离子,检验Fe2+离子的试剂为K3[Fe(CN)6],故答案为:b;
(5)浸出液E中存在AlO2—,首先通入足量的CO2要将AlO2—沉淀下来生成Al(OH)3,然后脱水生成Al2O3,故答案为:![]() Al(OH)3
Al(OH)3![]() Al2O3。
Al2O3。