��Ŀ����
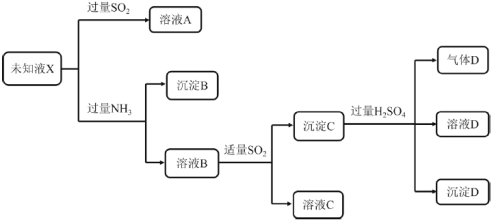
����Ŀ���������ʼ�ת���Ŀ�ͼ���ش��й����⣺

(1)д����ͼ������A��B��E��F�ֱ�ָ�����ʵĻ�ѧʽ��A��_____________ B��_____________ E��_____________ F��______________
(2)���2mol Na2O2������ˮ������Ӧ���ɵñ�״������������_________L��ͬʱ��Ӧ��ת�Ƶ���������____________��(NA��ʾ�����ӵ�����)
(3)���A��B�������3.0g(ƽ��Ħ������15g��mol��1)������G��ַ�Ӧ��ͨ������Na2O2�㣬��ʹNa2O2����__________g�����õ�O2_________mol��
���𰸡�H2 CO NaOH Na2CO3 22.4L 2NA 3.0 0.10
��������
C��H2O�ڸ����·�Ӧ����CO��H2����ת����ϵ��֪GΪO2��EӦΪNaOH��FΪNa2CO3����AΪH2��BΪCO��CΪH2O��DΪCO2��������ʵ����ʷ������
���ݿ�ͼ��ת����ϵ��AΪH2��BΪCO��CΪH2O��DΪCO2��EΪNaOH��FΪNa2CO3��GΪO2��
(1)�����Ϸ�����֪AΪH2��BΪCO��EΪNaOH��FΪNa2CO3���ʴ�Ϊ��H2��CO��NaOH��Na2CO3��
(2)����������������x��ת�Ƶ��ӵ����ʵ���Ϊy��
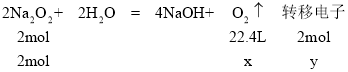
��x=22.4L��y=2mol����ĿΪ2NA���ʴ�Ϊ��22.4L��2NA��
(3)һ����̼��������������Ӧ���ɶ�����̼��ˮ��������̼��ˮ�ٺ������Ʒ�Ӧ����2H2+O2![]() 2H2O��2Na2O2+2H2O=4NaOH+O2��ӣ�H2+Na2O2=2NaOH��ͬ���ɵã�Na2O2+CO=Na2CO3�����Թ����������ص���CO��H2���������ʹ�����������3.0g����������һ����̼�����ʵ�����n1�����������ʵ�����n2����
2H2O��2Na2O2+2H2O=4NaOH+O2��ӣ�H2+Na2O2=2NaOH��ͬ���ɵã�Na2O2+CO=Na2CO3�����Թ����������ص���CO��H2���������ʹ�����������3.0g����������һ����̼�����ʵ�����n1�����������ʵ�����n2����![]() =15��������n1��n2=1��1���ɶ���������28n1+2n2=3.0���������n1=0.1mol��n2=0.1mol������Ԫ���غ�CO��H2��O2��Ӧ������0.1molCO2��0.1molH2O����2Na2O2+2H2O=4NaOH+O2 ��2Na2O2+2CO2=2Na2CO3+O2 ��֪���������������Ϊ
=15��������n1��n2=1��1���ɶ���������28n1+2n2=3.0���������n1=0.1mol��n2=0.1mol������Ԫ���غ�CO��H2��O2��Ӧ������0.1molCO2��0.1molH2O����2Na2O2+2H2O=4NaOH+O2 ��2Na2O2+2CO2=2Na2CO3+O2 ��֪���������������Ϊ![]() ��0.1mol+
��0.1mol+![]() ��0.1mol=0.1mol���ʴ�Ϊ��3.0��0.1��
��0.1mol=0.1mol���ʴ�Ϊ��3.0��0.1��

����Ŀ����ͼװ�ÿ������ռ�SO2����֤��ijЩ��ѧ���ʣ�����˵����ȷ���ǣ� ��

ѡ�� | �Լ� | ���� | ���� |
A | ����KMnO4��Һ | ��Һ��ɫ | SO2�������� |
B | Ʒ����Һ | ��Һ��ɫ | SO2��Ư���� |
C | ���з�̪��NaOH��Һ | ��Һ��ɫ | SO2��Ư���� |
D | ����ˮ��Һ | ��Һ����� | SO2�л�ԭ�� |
A. A B. B C. C D. D
����Ŀ��һ���¶��£���1 mol X��3 mol Y����2 L�ĺ����ܱ������У�������Ӧ��X(g)��3Y(g)2Z(g)����Ӧ�����в������������ʾ��
t/min | 0 | 10 | 20 | 30 | 40 |
p/kPa | 32 | 28.8 | 27.2 | 26.88 | 26.88 |
����˵����ȷ����
A.10minʱ����Y��ʾ��ƽ����Ӧ����Ϊ0.03 mol��L��1��min��1
B.X��Y��ת����֮�ȱ��ֲ���ʱ�����жϷ�Ӧ�ﵽƽ��״̬
C.ƽ��״̬ʱ��c(Z)��0.32 mol��L��1
D.�������ѹ�������ʵ���Ũ�ȼ���÷�Ӧ��ƽ�ⳣ������ֵ����