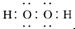题目内容
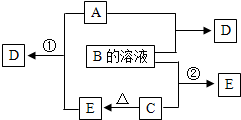 A、C为焰色反应呈黄色的两种化合物,且C是发酵粉的主要成分之一.B是实验室常用的一种强酸,D是有助燃性的单质气体,E能使澄清石灰水变混浊,但不能时品红溶液褪色.它们的相互转化关系如下图,其它产物已略去.
A、C为焰色反应呈黄色的两种化合物,且C是发酵粉的主要成分之一.B是实验室常用的一种强酸,D是有助燃性的单质气体,E能使澄清石灰水变混浊,但不能时品红溶液褪色.它们的相互转化关系如下图,其它产物已略去.(1)写出下列物质的化学式:A
(2)E是一种
(3)反应①的化学方程式是
(4)如果在密闭容器中将A、C以等物质的量混合,加热使其充分反应,最终容器中剩余固体的成分是
分析:A、C为焰色反应呈黄色的两种化合物,且C是发酵粉的主要成分之一,则C为NaHCO3,E能使澄清石灰水变混浊,但不能时品红溶液褪色,E为CO2,结合转化关系及B是实验室常用的一种强酸,D是有助燃性的单质气体可知,A为Na2O2,D为O2,B可能为盐酸,然后结合物质的性质及化学用语来解答.
解答:解:A、C为焰色反应呈黄色的两种化合物,且C是发酵粉的主要成分之一,则C为NaHCO3,E能使澄清石灰水变混浊,但不能时品红溶液褪色,E为CO2,结合转化关系及B是实验室常用的一种强酸,D是有助燃性的单质气体可知,A为Na2O2,D为O2,B可能为盐酸,
(1)由上述分析可知,A为Na2O2,C为NaHCO3,D为O2,故答案为:Na2O2;NaHCO3;O2;
(2)E为CO2,其电子式为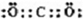 ,为直线分子,结构对称,为非极性分子,故答案为:非极性;
,为直线分子,结构对称,为非极性分子,故答案为:非极性;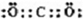 ;
;
(3)反应①的化学方程式是2Na2O2+2CO2=2Na2CO3+O2,反应②的离子方程式是HCO3-+H+=CO2↑+H2O,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;HCO3-+H+=CO2↑+H2O;
(4)将A、C以等物质的量混合,加热使其充分反应,2NaHCO3
2Na2CO3+CO2↑+H2O,2Na2O2+2CO2=2Na2CO3+O2、2Na2O2+2H2O=4NaOH+O2↑,若固体均为2mol,最终容器中剩余固体的成分是Na2CO3和NaOH,故答案为:Na2CO3和NaOH.
(1)由上述分析可知,A为Na2O2,C为NaHCO3,D为O2,故答案为:Na2O2;NaHCO3;O2;
(2)E为CO2,其电子式为
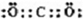 ,为直线分子,结构对称,为非极性分子,故答案为:非极性;
,为直线分子,结构对称,为非极性分子,故答案为:非极性;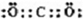 ;
;(3)反应①的化学方程式是2Na2O2+2CO2=2Na2CO3+O2,反应②的离子方程式是HCO3-+H+=CO2↑+H2O,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;HCO3-+H+=CO2↑+H2O;
(4)将A、C以等物质的量混合,加热使其充分反应,2NaHCO3
| ||
点评:本题为框图式无机推断题,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论,把握常见物质的性质即可解答,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目