题目内容
A、B、C、D、E为原子序数依次递增的四种短周期元素.A、D同族,B、C同周期.C、E组成的化合物既能够溶于硫酸又能够溶于D的水溶液.A、B两元素以4:1组成的化合物甲为气体,由A、C组成的两种化合物乙和丙都为液态,乙中A、C原子数之比为1:1,丙中为2:1,由D、C组成的两种化合物丁和戊都为固态,丁中D、C原子数之比为1:1,戊中为2:1.
回答下列问题:
(1)甲的名称
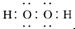 ;
;
(2)写出元素B的最高价氧化物和丁反应的化学方程式
(3)向含E离子的硫酸盐溶液中逐滴滴加戊溶于水所得的稀溶液,请写出该过程反应的离子方程式:
(4)甲与C的单质C2按一定比例混合放入含过量的丁密闭容器中,电火花引燃,维持温度在120℃,充分反应后容器内压强几乎为零,试写出符合题意的甲和C2的物质的量之比:
回答下列问题:
(1)甲的名称
甲烷
甲烷
;丙的分子式H2O
H2O
;丁中C元素的化合价-1
-1
;戊的焰色反应呈黄
黄
色;乙的电子式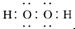
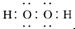
(2)写出元素B的最高价氧化物和丁反应的化学方程式
2Na2O2 +2CO2 =2Na2CO3 +O2
2Na2O2 +2CO2 =2Na2CO3 +O2
.(3)向含E离子的硫酸盐溶液中逐滴滴加戊溶于水所得的稀溶液,请写出该过程反应的离子方程式:
Al3++3OH-=Al(OH)3↓
Al3++3OH-=Al(OH)3↓
,Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.(4)甲与C的单质C2按一定比例混合放入含过量的丁密闭容器中,电火花引燃,维持温度在120℃,充分反应后容器内压强几乎为零,试写出符合题意的甲和C2的物质的量之比:
2:1
2:1
; 反应的化学方程式:2CH4+O2+6Na2O2=2Na2CO3+8NaOH
2CH4+O2+6Na2O2=2Na2CO3+8NaOH
.分析:A、B两元素以4:1组成的化合物甲为气体,则甲为CH4,A为H元素,B为C元素,由A、C组成的两种化合物乙和丙都为液态,乙中A、C原子数之比为1:1,丙中为2:1,则C为O元素,形成的化合物分别为H2O2、H2O,由D、C组成的两种化合物丁和戊都为固态,丁中D、C原子数之比为1:1,戊中为2:1,则D为Na元素,形成的化合物分别为Na2O2、Na2O,C、E组成的化合物既能够溶于硫酸又能够溶于D的水溶液,说明E为Al元素,形成的化合物Al2O3具有两性,根据元素所在周期表中的位置结合元素周期律的递变规律来解答元素、原子以及对应化合物的结构和性质.
解答:解:A、B两元素以4:1组成的化合物甲为气体,则甲为CH4,A为H元素,B为C元素,由A、C组成的两种化合物乙和丙都为液态,乙中A、C原子数之比为1:1,丙中为2:1,则C为O元素,形成的化合物分别为H2O2、H2O,由D、C组成的两种化合物丁和戊都为固态,丁中D、C原子数之比为1:1,戊中为2:1,则D为Na元素,形成的化合物分别为Na2O2、Na2O,C、E组成的化合物既能够溶于硫酸又能够溶于D的水溶液,说明E为Al元素,形成的化合物Al2O3具有两性.
(1)由以上分析可知,甲为CH4,丙为H2O,丁为Na2O2,O元素的化合价为-1价,戊为Na2O,含有Na元素,焰色反应呈黄色,乙为H2O2,电子式为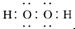 ,故答案为:甲烷;H2O;-1;黄;
,故答案为:甲烷;H2O;-1;黄;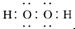 ;
;
(2)元素B的最高价氧化物为CO2 ,丁为Na2O2,二者反应的化学方程式为2Na2O2 +2CO2 =2Na2CO3 +O2,
故答案为:2Na2O2 +2CO2 =2Na2CO3 +O2;
(3)含Al3+离子的硫酸盐溶液中逐滴滴加NaOH的稀溶液,先生成Al(OH)3沉淀,Al(OH)3具有两性,能继续与NaOH反应生成AlO2-,反应的离子方程式为Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=AlO2-+2H2O;
(4)甲烷与氧气通入到含过量的Na2O2 密闭容器中,电火花引燃,维持温度在120℃,充分反应后容器内压强几乎为零,则参加反应的气体全部生成固体,根据质量守恒可知生成物应为Na2CO3和NaOH,根据甲烷的组成可知Na2CO3与NaOH物质的量之比为1:4,反应的方程式为2CH4+O2+6Na2O2=2Na2CO3+8NaOH,由方程式可知甲烷和氧气的物质的量之比为2:1,
故答案为:2:1;2CH4+O2+6Na2O2=2Na2CO3+8NaOH.
(1)由以上分析可知,甲为CH4,丙为H2O,丁为Na2O2,O元素的化合价为-1价,戊为Na2O,含有Na元素,焰色反应呈黄色,乙为H2O2,电子式为
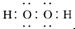 ,故答案为:甲烷;H2O;-1;黄;
,故答案为:甲烷;H2O;-1;黄;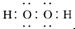 ;
;(2)元素B的最高价氧化物为CO2 ,丁为Na2O2,二者反应的化学方程式为2Na2O2 +2CO2 =2Na2CO3 +O2,
故答案为:2Na2O2 +2CO2 =2Na2CO3 +O2;
(3)含Al3+离子的硫酸盐溶液中逐滴滴加NaOH的稀溶液,先生成Al(OH)3沉淀,Al(OH)3具有两性,能继续与NaOH反应生成AlO2-,反应的离子方程式为Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=AlO2-+2H2O;
(4)甲烷与氧气通入到含过量的Na2O2 密闭容器中,电火花引燃,维持温度在120℃,充分反应后容器内压强几乎为零,则参加反应的气体全部生成固体,根据质量守恒可知生成物应为Na2CO3和NaOH,根据甲烷的组成可知Na2CO3与NaOH物质的量之比为1:4,反应的方程式为2CH4+O2+6Na2O2=2Na2CO3+8NaOH,由方程式可知甲烷和氧气的物质的量之比为2:1,
故答案为:2:1;2CH4+O2+6Na2O2=2Na2CO3+8NaOH.
点评:本题考查元素的位置结构性质的相互关系及应用,题目难度中等,注意根据常见化合物的形式推断元素的种类,注重基础知识的积累.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
【化学--选修3:物质结构与性质】
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)G位于 族 区,价电子排布式为 .
(2)B基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈
形.
(3)画出C原子的电子排布图 .
(4)已知BA5为离子化合物,写出其电子式 .
(5)DE3中心原子的杂化方式为 ,用价层电子对互斥理论推测其空间构型为 .
(6)用电子式表示F元素与E元素形成化合物的形成过程 .
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
形.
(3)画出C原子的电子排布图
(4)已知BA5为离子化合物,写出其电子式
(5)DE3中心原子的杂化方式为
(6)用电子式表示F元素与E元素形成化合物的形成过程
 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:

