��Ŀ����
����Ŀ�����Ȼ����Ǻϳɲ���������Ҫԭ�ϣ�
��1�����ù�ҵFeCl3��ȡ�����IJ���������[Fe2��C2O4��35H2O]��ʵ��������ͼ��ʾ�� 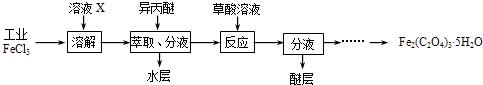
��Ϊ����FeCl3ˮ�⣬��ҺXΪ ��
������������FeCl3�ܱ��������ȡ����ԭ������������ȡ����Һ������ˮ�����Ƿ���Fe3+�ķ����� ��
������Fe2��C2O4��35H2O���ñ�ˮϴ�ӣ���Ŀ���� ��
��Ϊ�ⶨ���ò���������Ĵ��ȣ�ʵ���ҳ�ȡa g��Ʒ���������ữ����KMnO4����Һ�ζ����ɵ�H2C2O4 �� KMnO4����ҺӦ������ͼ��ʾ��������ס����ҡ����У�������������ʵ����Fe2��C2O4��35H2O����ƫ�͵��� ��
a��ʢ��KMnO4�ĵζ���ˮϴ��δ�ñ�Һ��ϴ
b���ζ��ܵζ�ǰ���첿�������ݣ��ζ�����ʧ
c���ζ�ǰ���Ӷ������ζ����Ӷ���
��2��ij�о���ѧϰС������ʴ�̶�ͭ��·�����÷�Һ������ΪFeCl2��CuCl2��FeCl3���������Ʊ�����ͭ����ˮFeCl3 �� ����FeCl3�ϳ�Fe2��C2O4��35H2O���벹��������ʴ�̷�Һ�Ʊ�����ͭ����ˮFeCl3��ʵ�鲽�裨��ѡ�õ��Լ������ۡ����ᡢNaOH��Һ��H2O2��Һ�������Һ�м����������ۣ���ַ�Ӧ����ˣ���������ҺpH������Һ����Ũ������ȴ�ᾧ�����ˡ�ϴ�Ӹ����FeCl36H2O�� �� �õ���ˮFeCl3 �� ![]()
���𰸡�
��1����Ũ�����FeCl3��������е��ܽ�ȴ�������ˮ�е��ܽ�ȣ�ȡ������Һ�������еμ�����KSCN��Һ������Һ��죬����Fe3+����ȥ���ʡ����ٲ�����������ܽ���ģ��ף�c
��2���������м�������HCl����ַ�Ӧ����ˡ�ϴ�ӡ������ͭ�ۣ������ι���������Һ�ϲ��������м�������H2O2��Һ��Fe2+ȫ������Fe3+����FeCl3?6H2O��HCl�������м�����ˮ
���������⣺��1�����ữFeCl3�������ữ�����������ʣ������������ӵ�ˮ�⣬���Դ��ǣ���Ũ���������ȡ�����������ڲ�ͬ�ܼ��е��ܽ�Ȳ��������ȡ���ʵ�һ�ַ���������ȡ˵��FeCl3��������е��ܽ�ȴ�������ˮ�е��ܽ�ȣ�����Fe3+��KSCN��ҺЧ����ã����Դ��ǣ�FeCl3��������е��ܽ�ȴ�������ˮ�е��ܽ�ȣ�ȡ������Һ�������еμ�����KSCN��Һ������Һ��죬����Fe3+����ϴ���dz�ȥ�����������ʣ���ˮ�Ǽ��ٳ����ܽ���ʧ�����Դ��ǣ���ȥ���ʡ����ٲ�����������ܽ���ģ���KMnO4����Һ����ǿ�����ԣ�Ӧ������ʽ�ζ����У�a��û����ϴ���¸������Ũ�ȵ���������࣬ƫ�ߣ�
b�����������������࣬ƫ�ߣ�
c���������ƫС�����ƫ�ͣ���ȷ��
���Դ��ǣ��ף�c����2���ù��������������������˫��ˮ����Ϊ�����ӣ���ʵ���Ŀ���ǵõ�ͭ���ʣ���Ӧ���ɵ���ͭ��ʣ�����Ļ�������������ȥͭ�е��������ѷ�Ӧ��Һ��ǰ�κϲ����ʲ���Ϊ�������м�������HCl����ַ�Ӧ����ˡ�ϴ�ӡ������ͭ�ۣ������ι���������Һ�ϲ��������м�������H2O2��Һ��Fe2+ȫ������Fe3+��ֱ�Ӽ���FeCl36H2O��ˮ�⣬Ϊ����ˮ������HCl��Χ�½��У�
���Դ��ǣ��������м�������HCl����ַ�Ӧ����ˡ�ϴ�ӡ������ͭ�ۣ������ι���������Һ�ϲ��������м�������H2O2��Һ��Fe2+ȫ������Fe3+����FeCl36H2O��HCl�������м�����ˮ��

 �żӾ���ϵ�д�
�żӾ���ϵ�д�����Ŀ�����¶�T1��T2ʱ���ֱ�0.50mol CH4��1.20mol NO2�������Ϊ1L���ܱ������У��������·�Ӧ��CH4��g��+2NO2��g��N2��g��+CO2��g��+2H2O��g�������n��CH4����ʱ��仯�������±���
ʱ��/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n��CH4��/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n��CH4��/mol | 0.50 | 0.30 | 0.18 | �� | 0.15 |
����˵����ȷ���ǣ� ��
A.T2ʱCH4��ƽ��ת����Ϊ70.0%
B.�÷�Ӧ�ġ�H��0��T1��T2
C.���������������䣬T1ʱ��ƽ����ϵ���ٳ���0.30 mol CH4��0.80 mol H2O��g����ƽ��������Ӧ�����ƶ�
D.���������������䣬T1ʱ��ƽ����ϵ���ٳ���0.50 mol CH4��1.20 mol NO2 �� ��ԭƽ����ȣ�����ƽ��ʱN2��Ũ���������������С
����Ŀ������˵����ȷ���ǣ� ��
A | B | C | D |
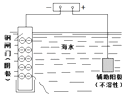
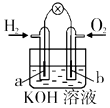
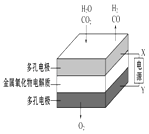
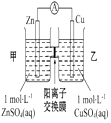
��բ�����ױ���ʴ | a��b��Ϊ���Ե缫��b����Ӧ�ǣ�O+4OH����4e��=2H2O | �������������ɵ���������ʵ���֮����1��1 | ��ع���һ��ʱ�� |
|
|
|
|
A.A
B.B
C.C
D.D