题目内容
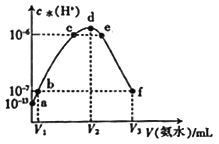
【题目】常温下,向20 mL的某稀盐酸中滴入0.1 mol·L-1的氨水,溶液中由水电离出的氢离子浓度随滴人氨水体积的变化如图。下列分析不正确的是
A. V2=20 mL
B. d点溶液中:c(NH4+)>c(Cl-)
C. b点溶液中:c(H+)=c(OH-)
D. 该稀盐酸的浓度为0.1mol/L
【答案】BC
【解析】A、d点水电离出的氢离子浓度最大,此时恰好反应生成氯化铵,铵根水解,因此V2=20 mL
,A正确;B、d点水电离出的氢离子浓度最大,此时恰好反应生成氯化铵,铵根水解,溶液显酸性,因此d点溶液中:c(NH4+)<c(Cl-),B错误;C、b点氨水不足,盐酸过量,溶液显酸性,则b点溶液中:c(H+)>c(OH-),C错误;D、根据20mL稀盐酸溶液中,水电离出的氢离子浓度是10-13mol/L,根据水的离子积得到盐酸电离出的氢离子浓度是0.1mol/L,稀盐酸的浓度为0.1mol/L,D正确;答案选BC。

【题目】工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度 | ||
500℃ | 700℃ | 800℃ | ||
①2H2(g)+CO(g)CH3OH(g) | K1 | 2.5 | 0.34 | 0.15 |
②H2(g)+CO2(g)H2O(g)+CO(g) | K2 | 1 | 1.7 | 2.52 |
③3H2(g)+CO2(g)CH3OH(g)+H2O(g) | K3 | |||
请回答下列问题:
(1)判断反应①是________(填“吸热”或“放热”)反应
(2)据据反应①与反应②可推导出K1、K2与K3之间的关系,则K3 =________(用K1、K2表示)
(3)某温度下反应①式中各物质的平衡浓度符合下式:20c(CH3OH) = 3c(CO)·c2(H2),试判断此时的温度为________。
(4)500℃时测得反应③在某时刻H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度分别为0.4 mol·L-1、1 mol·L-1、0.5 mol·L-1、0.4 mol·L-1,则此时ν(正)________ν(逆)(填“>”、“=”或“<”)。
(5)一定条件下将H2(g)和CO2(g)以体积比3:1置于恒温恒容的密闭容器发生反应③,下列能说明该反应达到平衡状态的有_____________
A.体系密度保持不变
B.H2和CO2的体积比保持不变
C.混合气体的平均相对分子量不变时,反应一定达到平衡状态
D.当破坏CO2中2个碳氧双键,同时破坏H2O 中的2个氧氢键,反应一定达到平衡状态
(6)若500℃时在2L密闭容器中加入2molH2和amolCO2进行②的反应,反应5min后达到平衡,平衡时CO2的转化率为50%,求a =________mol,用H2表示该反应达到平衡时的平均反应速率ν(H2) =________mol·L-1·min-1




