题目内容
17.下列有关化学用语使用正确的是( )| A. | 硫原子的原子结构示意图: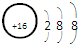 | |
| B. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| C. | NH4Cl的电子式: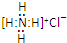 | |
| D. | 高氯酸(HClO4)中氯元素的化合价为+5 |
分析 A.硫原子核电荷数、核外电子数都是16,核外电子数不是18;
B.氧元素的质子数为8,中子数为10的氧原子的质量数是18;
C.氯化铵为离子晶体,由氨根离子与氯离子通过离子键结合在一起;
D.高氯酸的Cl处于最高价.
解答 解:A. 表示的是硫离子,硫原子的核外电子数为16,硫原子结构示意图为:
表示的是硫离子,硫原子的核外电子数为16,硫原子结构示意图为: ,故A错误;
,故A错误;
B.含有10个中子的氧原子的质量数为18,该氧原子可以表示为:818O,故B正确;
C.氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为: ,故C错误;
,故C错误;
D.高氯酸的Cl处于最高价,为+7价,故D错误,故选B.
点评 本题考查了电子式、原子结构示意图、化学式等表示方法的判断,题目难度中等,注意掌握电子式、原子结构示意图等化学用语的概念及表示方法,明确离子化合物与共价化合物的电子式区别.

练习册系列答案
相关题目
12.某铝厂的有毒废水流入多瑙河分支,大量死鱼出现在拉巴河和多瑙河的交汇处,这里河水的pH高达9.1.为了拯救多瑙河的生态环境,必须将河水的pH降至8以下.因此可向河水中投入食醋、熟石膏(CaSO4)等来降低碱性.下列有关说法正确的是( )
| A. | 在元素周期表中,铝的周期数是其主族序数的2倍 | |
| B. | 铝原子的基态电子排布图为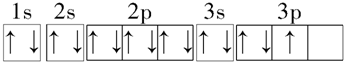 | |
| C. | 同周期,铝、钙所在主族的元素的原子序数之差只为1或11 | |
| D. | 工业上冶炼金属铝的方法是电解熔融的Al2O3 |
9.卤代烃的取代反应,实质是带负电荷的原子团取代了卤代烃中的卤原子,如CH3Br+OH-(或NaOH)→CH3OH+Br-(或NaBr),下列化学方程式中不正确的是( )
| A. | CH3CH2Br+NaHS→CH3CH2SH+NaBr | |
| B. | CH3I+CH3ONa→CH3OCH3+NaI | |
| C. | CH3CH2Cl+CH3ONa→CH3CH2ONa+CH3Cl | |
| D. | CH3CH2Cl+CH3CH2ONa→(CH3CH2)2O+NaCl |
7.①制备纳米TiO2的方法之一是TiCl4水解生成TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2.
②用NaOH测定滤液的浓度:准确称量1.000gNaOH固体质量,配制成250mL溶液,准确量取25.00mL溶液装在锥形瓶,滴加2滴酚酞作指示剂.把滤液装在酸式滴定管中,调节液面排除气泡后,滤液的凹液面刚好在“0”刻度,滴定NaOH溶液,达到终点记录读数.实验重复3次.记录见下表.
(1)TiCl4水解生成TiO2•xH2O的化学方程式为TiCl4+(x+2)H2O=TiO2•xH2O↓+4HCl
(2)配制成250mL溶液使用的量具是250mL容量瓶;
(3)滴定终点的现象是浅红色溶液变为无色,半分钟内不变色.
(4)滤液中溶质的物质的量浓度为0.125mol•L-1.
(5)若在滴定终点读取滴定管刻度时,俯视标准液液面,使对测定结果偏高. (填“偏高”、“偏低”或“无影响”)
②用NaOH测定滤液的浓度:准确称量1.000gNaOH固体质量,配制成250mL溶液,准确量取25.00mL溶液装在锥形瓶,滴加2滴酚酞作指示剂.把滤液装在酸式滴定管中,调节液面排除气泡后,滤液的凹液面刚好在“0”刻度,滴定NaOH溶液,达到终点记录读数.实验重复3次.记录见下表.
| 滴定次数 | NaOH溶液体积/mL | 滴定消耗滤液体积/mL |
| 1 | 25.00 | 20.02 |
| 2 | 25.00 | 17.10 |
| 3 | 25.00 | 19.98 |
(2)配制成250mL溶液使用的量具是250mL容量瓶;
(3)滴定终点的现象是浅红色溶液变为无色,半分钟内不变色.
(4)滤液中溶质的物质的量浓度为0.125mol•L-1.
(5)若在滴定终点读取滴定管刻度时,俯视标准液液面,使对测定结果偏高. (填“偏高”、“偏低”或“无影响”)
8.下列各组物质中,属于同分异构体的一组是( )
| A. | 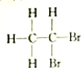 和 和 | B. | 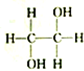 和 和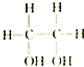 | C. | 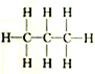 和 和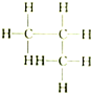 | D. | CH3-CH2-CHO和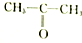 |

 .
.
 .
.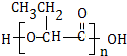 .
.