题目内容
【题目】某传感器工作原理如图所示。利用该传感器可以测定空气中NO、CO、NH3、SO2等有害气体的含量。下列说法正确的是
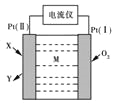
A. 传感器工作中,电子由Pt(Ⅰ)极经电流仪传到Pt(Ⅱ)极
B. 若M为熔融KOH,X为NH3,Y为N2,则负极的电极反应式为2NH3-6e- = N2+6H+
C. 若M是含O2-的固体电解质,X为NO,则正极的电极反应式为O2 + 4e- = 2O2-
D. 若X为CO,M为KOH溶液,则电池总反应为2CO+O2 = 2CO2
【答案】C
【解析】
A.题述装置属于原电池,Pt(Ⅰ)极为正极,Pt(Ⅱ)极为负极,电子由负极经外电路流向正极,故A错误;
B.由于M是熔融的KOH,即使放电生成H+也会与OH-反应生成水,所以负极的电极反应式为2NH3-6e- +6OH-= N2+6H2O ,故B错误;
C.若M是含O2-的固体电解质,则负极的电极反应式为2NO-4 e- +2O2-=2NO2,正极的电极反应式为O2 + 4e- = 2O2-,故C正确;
D.若X为CO,M为KOH溶液,则负极的电极反应式为CO-2e- +4OH-=CO32-+2H2O,电池总反应为2CO+4KOH+O2=2K2CO3+2H2O,故D错误。
故答案选C。

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目