题目内容
已知FeS+2HCl══FeCl2+H2S↑,将8.8gFeS固体置于200mL2.0mol×L-1的盐酸中,以制备H2S气体,反应完全后,若溶液中H2S的浓度为0.10mol×L-1,假定溶液体积不变,试计算:
(1)收集到的H2S气体的体积(标准状况);
(2)溶液中Fe2+和H+的物质的量浓度。
答案:

练习册系列答案
相关题目
[2012·潍坊一模] (14分)黄铜矿的主要成分是CuFeS2,是工业炼铜的主要原料。已知黄铜矿在空气中焙烧生成Cu、FeS和SO2,FeS+2HCl=FeCl2+H2S↑,H2S是一种剧毒气体。某科研小组设计以黄铜矿为原料制取单质铜和氯化铁晶体(FeCl3·6H2O)的流程如下:

(1)92gCuFeS2在空气中焙烧生成Cu、FeS和SO2转移电子的物质的量为 。
(2)请简述检验气体Ⅰ的操作步骤 。
(3)在实验室中,欲用38%(密度为1.18g·mL-1)的盐酸配制30%的盐酸,需要的玻璃仪器主要有 。
(4)气体Ⅲ最好选用 (填写序号),其主要作用是 。
| A.O2 | B.H2 | C.Cl2 | D.N2 |

装置A中发生反应的离子方程式为 。
选用合适装置导管口的连接顺序为a接 。图中仪器G的名称是 ;在使用该仪器时,应首先 。


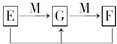 已知A、B、C、D两种短周期元素,分别属于不同的主族,其原子序数依次增大,其中A与D、B与C的原子的最外层电子数之和均为9,A原子的最外层与次外层电子数相等,A、B、C、D中只有两种金属元素.试回答下列问题:
已知A、B、C、D两种短周期元素,分别属于不同的主族,其原子序数依次增大,其中A与D、B与C的原子的最外层电子数之和均为9,A原子的最外层与次外层电子数相等,A、B、C、D中只有两种金属元素.试回答下列问题: