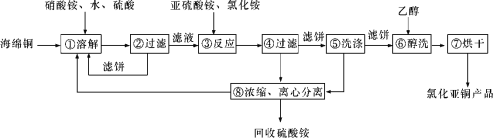
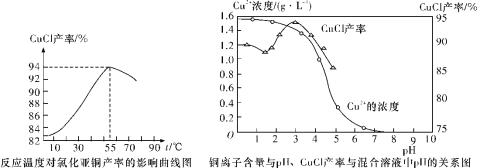
题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,2.24 L己烷中共价键数目为1.9NA
B.2 L 0.5 mol/L亚硫酸溶液中含有的H+数为2NA
C.高温下,16.8 g Fe与足量的水蒸气完全反应转移的电子数为0.8NA
D.在密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA
【答案】C
【解析】
A.标准状况下,己烷为液态物质,无法利用体积计算其中共价键数目,故A错误;
B. H2SO3为弱酸,在水中部分电离,2 L 0.5 mol/L亚硫酸溶液中含有的H+数小于2NA,故B错误;
C.高温下,16.8 g Fe物质的量![]() ,与足量的水蒸气完全反应生成Fe3O4,铁元素化合价平均升高
,与足量的水蒸气完全反应生成Fe3O4,铁元素化合价平均升高![]() 价,则转移的电子数为
价,则转移的电子数为![]() ,故C正确;
,故C正确;
D. 在密闭容器中2 mol NO与1 mol O2充分反应![]() ,反应为可逆反应,产物的分子数介于2NA~3NA之间,故D错误;
,反应为可逆反应,产物的分子数介于2NA~3NA之间,故D错误;
故答案选:C。

【题目】回答下列问题:
I.乳酸(![]() )、酒精、醋酸、淀粉等都是生活中常见的物质。
)、酒精、醋酸、淀粉等都是生活中常见的物质。
(1)在生活中,常选择上述物质中_______________(填结构简式)清洗水壶里的水垢。
(2)生活中常选择_______________酒精![]() 选择“75%”“95%”或“无水”
选择“75%”“95%”或“无水”![]() 皮肤消毒。
皮肤消毒。
(3)上述物质中,属于天然高分子化合物的是_________________![]() 填名称
填名称![]() 。
。
(4)乳酸中发生如下变化:![]() ,则所用的试剂a为________(写化学式)。
,则所用的试剂a为________(写化学式)。
II.X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
元素 | 相关信息 |
X | X的最外层电子数是次外层的2倍 |
Y | M层上的电子数是K层的3倍 |
Z | Z的一种核素的质量数为53,中子数为34 |
W | W2+与氖原子具有相同核外电子排布 |
(5)X在元素周期表中的位置为___________;Y元素的名称为________________。
(6)元素W的离子结构示意图是_______________;Z、Y形成的化合物为____________(用化学式表示)。