题目内容
A.(1)请写出以乙烯为有机原料合成乙酸乙酯的各步反应方程式,并注明反应类型.
(2)下表是A、B二种有机物的有关信息;
根据表中信息回答下列问题:
①A的结构简式为
②写出在浓硫酸作用下A发生消去反应的化学方程式
③B具有的性质是
a.无色无味液体; b.有毒; c.不溶于水; d.密度比水大; e.与酸性KMnO4 溶液和溴水反应褪色; f.任何条件下不与氢气反应;
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: +HNO3(浓)
+HNO3(浓)

 +HNO3(浓)
+HNO3(浓)
 .
.
CH2=CH2+H2O
CH3CH2OH
| 催化剂 |
CH2=CH2+H2O
CH3CH2OH
:加成反应| 催化剂 |
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
| 浓硫酸 |
| △ |
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
:| 浓硫酸 |
| △ |
酯化反应
酯化反应
2CH3CHO+O2
2CH3COOH
| 催化剂 |
2CH3CHO+O2
2CH3COOH
:氧化反应| 催化剂 |
(2)下表是A、B二种有机物的有关信息;
| A | B |
| ①分子式为C3H8O; ②在Cu的作用下催化氧化的产物 不能发生银镜反应 |
①由C、H两种元素组成; ②球棍模型为:  |
①A的结构简式为
CH3CH(OH)CH3
CH3CH(OH)CH3
.②写出在浓硫酸作用下A发生消去反应的化学方程式
CH3CH(OH)CH3
CH2=CHCH3+H2O
| 浓H2SO4 |
| △ |
CH3CH(OH)CH3
CH2=CHCH3+H2O
.| 浓H2SO4 |
| △ |
③B具有的性质是
bc
bc
(填序号):a.无色无味液体; b.有毒; c.不溶于水; d.密度比水大; e.与酸性KMnO4 溶液和溴水反应褪色; f.任何条件下不与氢气反应;
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
 +HNO3(浓)
+HNO3(浓)| 浓H2SO4 |
| △ |

 +HNO3(浓)
+HNO3(浓)| 浓H2SO4 |
| △ |

分析:(1)乙烯和水发生加成反应生成乙醇,乙醇在Cu、加热条件下发生催化氧化生成乙醛,乙醛进一步氧化为乙酸,乙醇与乙酸发生酯化反应成乙酸乙酯;
(2)A分子式为C3H8O,在Cu的作用下催化氧化的产物,不能发生银镜反应,则A中含有-OH,为2-丙醇,在浓硫酸、加热条件下发生消去反应生成乙烯;
根据B的组成元素及其球棍模型知,B的分子式为C6H6,是苯.
(2)A分子式为C3H8O,在Cu的作用下催化氧化的产物,不能发生银镜反应,则A中含有-OH,为2-丙醇,在浓硫酸、加热条件下发生消去反应生成乙烯;
根据B的组成元素及其球棍模型知,B的分子式为C6H6,是苯.
解答:解:(1)乙烯为有机原料合成乙酸乙酯的步骤为:乙烯和水发生加成反应生成乙醇,乙醇在Cu、加热条件下发生催化氧化生成乙醛,乙醛进一步氧化为乙酸,乙醇与乙酸发生酯化反应成乙酸乙酯,各步反应方程式依次为:
①CH2=CH2+H2O
CH3CH2OH,该反应为加成反应;
②2CH3CH2OH+O2
2CH3CHO+2H2O,属于氧化反应;
③2CH3CHO+O2
2CH3COOH,属于氧化反应;
④CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,属于酯化反应;
故答案为:CH2=CH2+H2O
CH3CH2OH,加成反应;
2CH3CH2OH+O2
2CH3CHO+2H2O,氧化反应;
2CH3CHO+O2
2CH3COOH,氧化反应;
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,酯化反应;
(2)A分子式为C3H8O,在Cu的作用下催化氧化的产物,不能发生银镜反应,则A中含有-OH,为2-丙醇,在浓硫酸、加热条件下发生消去反应生成乙烯;
根据B的组成元素及其球棍模型知,B的分子式为C6H6,是苯.
①通过以上分析知,A是2-丙醇,则A的结构简式为CH3CH(OH)CH3,
故答案为:CH3CH(OH)CH3;
②浓硫酸作用下A发生消去反应生成丙烯,则该反应的化学方程式为CH3CH(OH)CH3
CH2=CHCH3+H2O,
故答案为:CH3CH(OH)CH3
CH2=CHCH3+H2O;
③B是苯,苯是无色有特殊气味的液体,有毒,不溶于水,且密度小于水,与酸性高锰酸钾溶液和溴水都不反应,在一定条件下能和氢气发生加成反应生成环己烷,故选bc;
在浓硫酸作用下,苯和浓硝酸发生取代反应生成硝基苯,反应方程式为:
 +HNO3(浓)
+HNO3(浓)
 ,
,
故答案为: +HNO3(浓)
+HNO3(浓)
 .
.
①CH2=CH2+H2O
| 催化剂 |
②2CH3CH2OH+O2
| Cu |
| △ |
③2CH3CHO+O2
| 催化剂 |
④CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
故答案为:CH2=CH2+H2O
| 催化剂 |
2CH3CH2OH+O2
| Cu |
| △ |
2CH3CHO+O2
| 催化剂 |
CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
(2)A分子式为C3H8O,在Cu的作用下催化氧化的产物,不能发生银镜反应,则A中含有-OH,为2-丙醇,在浓硫酸、加热条件下发生消去反应生成乙烯;
根据B的组成元素及其球棍模型知,B的分子式为C6H6,是苯.
①通过以上分析知,A是2-丙醇,则A的结构简式为CH3CH(OH)CH3,
故答案为:CH3CH(OH)CH3;
②浓硫酸作用下A发生消去反应生成丙烯,则该反应的化学方程式为CH3CH(OH)CH3
| 浓H2SO4 |
| △ |
故答案为:CH3CH(OH)CH3
| 浓H2SO4 |
| △ |
③B是苯,苯是无色有特殊气味的液体,有毒,不溶于水,且密度小于水,与酸性高锰酸钾溶液和溴水都不反应,在一定条件下能和氢气发生加成反应生成环己烷,故选bc;
在浓硫酸作用下,苯和浓硝酸发生取代反应生成硝基苯,反应方程式为:
 +HNO3(浓)
+HNO3(浓)| 浓H2SO4 |
| △ |
 ,
,故答案为:
 +HNO3(浓)
+HNO3(浓)| 浓H2SO4 |
| △ |
 .
.点评:本题考查有机物的合成,难度不大,掌握官能团的性质与转化是关键,旨在考查学生对基础知识的掌握.

练习册系列答案
相关题目
 CH2=CH2+R1CH=CHR2
CH2=CH2+R1CH=CHR2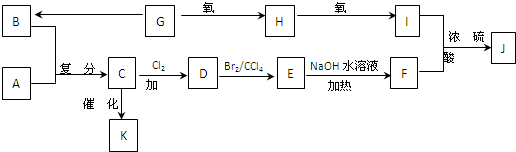


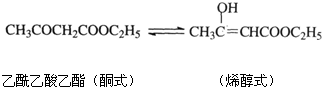
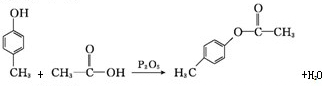
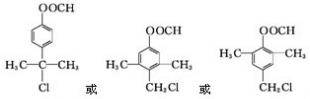
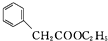 )是一种重要的化工原料.请写出以苯、甲醛和乙醇为主要原料制备苯乙酸乙酯的合成路线流程图
)是一种重要的化工原料.请写出以苯、甲醛和乙醇为主要原料制备苯乙酸乙酯的合成路线流程图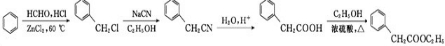

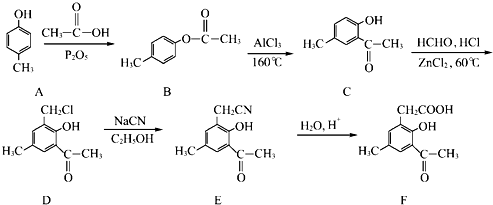
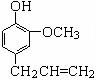 丁子香酚存在于丁香油、樟脑油等中,常用于配制康乃馨型香精以及制异丁香酚和香兰素等,也用作杀虫剂和防腐剂.丁子香酚结构简式如图:
丁子香酚存在于丁香油、樟脑油等中,常用于配制康乃馨型香精以及制异丁香酚和香兰素等,也用作杀虫剂和防腐剂.丁子香酚结构简式如图: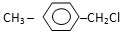 和乙醇为原料制备丁子香酚的一种同分异构体.对-甲基苯甲酸乙酯
和乙醇为原料制备丁子香酚的一种同分异构体.对-甲基苯甲酸乙酯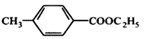 的合成路线(无机试剂任选).(合成路线常用的表示方式为:A
的合成路线(无机试剂任选).(合成路线常用的表示方式为:A