题目内容
14. 某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如
某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断正确的是( )
| A. | Ⅱ为盐酸稀释时的pH变化曲线 | |
| B. | b点酸的浓度小于a点酸的浓度 | |
| C. | b点溶液的导电性比c点溶液的导电性弱 | |
| D. | a点Kw的数值比c点Kw的数值小 |
分析 根据盐酸是强酸,完全电离,醋酸是弱酸,部分电离,相同温度下,相同pH值的盐酸和醋酸溶液,醋酸浓度大,溶液稀释时,醋酸进一步电离,其溶液中离子浓度大于盐酸的离子浓度,故II应为醋酸稀释时的pH值变化曲线,利用c点、b点溶液中的离子浓度来分析导电性;Kw只与温度有关,与溶液的种类以及浓度大小没有关系;相同pH值的盐酸和醋酸,稀释到相同体积时,醋酸(II)浓度大于盐酸(I)浓度.
解答 解:A、Ⅱ应为醋酸稀释时的pH值变化曲线,故A错误;
B、相同pH值的盐酸和醋酸,醋酸浓度远大于盐酸的浓度,稀释到相同体积时,醋酸(Ⅱ)浓度大于盐酸(Ⅰ)浓度,故B正确;
C、溶液导电性取决于离子浓度,b点的H+浓度大,导电性强,故C错误;
D、Kw的大小只取决于温度,a、c温度一样,a点Kw的数值和c点的一样,故D错误;
故选B.
点评 本题考查强弱电解质溶液稀释时的浓度变化,注意加水促进弱电解质电离的特点.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
4.学好自然科学知识是改造自然的基础.自然科学知识告诉我们,物质的能量越低,该物质越稳定.下列含氮物质中,能量最低的是( )
| A. | 氨气 | B. | 氮气 | C. | 一氧化氮 | D. | 硝酸 |
5. 在一密闭容器中通入A、B两种气体,一定条件下发生如下反应:2A(g)+B(g)?3C(g);△H<0,达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )
在一密闭容器中通入A、B两种气体,一定条件下发生如下反应:2A(g)+B(g)?3C(g);△H<0,达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )
 在一密闭容器中通入A、B两种气体,一定条件下发生如下反应:2A(g)+B(g)?3C(g);△H<0,达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )
在一密闭容器中通入A、B两种气体,一定条件下发生如下反应:2A(g)+B(g)?3C(g);△H<0,达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )| X | Y | |
| A | 增大压强 | C的体积分数 |
| B | 使用催化剂 | C的平衡浓度 |
| C | 充入A | B的转化率 |
| D | 降低温度 | 超过活化能Ea的活化分子百分数 |
| A. | A | B. | B | C. | C | D. | D |
2.下列不属于有机物的是( )
| A. | 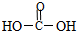 | B. | CCl4 | C. | 蔗糖 | D. | 合成纤维 |
9.下列实验操作不正确的是( )
| A. | 用容量瓶配制100ml 2.000mol/L的NaCl | |
| B. | 用分液漏斗分离乙醇和水 | |
| C. | 用烧杯溶解FeCl3试样 | |
| D. | 用电子天平称量NaCl固体5.85g |
19.下列有关化学反应与能量变化的叙述正确的是( )
| A. | 铝与氧化铁反应既是氧化还原反应,又是吸热反应 | |
| B. | 化学反应中的能量变化只体现为热量的形式 | |
| C. | Ca O+H2O=Ca (OH)2反应过程中,旧键断裂吸收的能量小于新键形成释放的能量 | |
| D. | 外界条件相同时,放热反应的速率一定大于吸热反应的速率 |
6.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,11.2L HF中含有分子的数目为0.5NA | |
| B. | 0.1molFe与少量氯气反应生成FeCl2,转移电子数为0.2NA | |
| C. | 1.4g 由乙烯和环丙烷组成的混合物中含有原子的数目为 0.3NA | |
| D. | 0.1 mol•L-1碳酸钠溶液中含有CO32-离子数目小于0.1 NA |
3.NA表示阿伏加德罗常数,下列判断正确的是( )
| A. | 6.8g熔融的KHSO4中含有阳离子数0.05NA | |
| B. | 1mol冰醋酸和lmo1乙醇经催化加热反应可生成H2O分子数为NA | |
| C. | 乙烯和环丙烷(C3H6)组成的28g混合气体中含有3NA个氢原子 | |
| D. | 常温常压下,17g羟基中含有的电子数为10NA |
