题目内容
已知在一定条件下, 2SO2+O2 2SO3 反应达平衡后SO2的转化率为45.3%,加入V2O5(催化剂)后,SO2的转化率为
2SO3 反应达平衡后SO2的转化率为45.3%,加入V2O5(催化剂)后,SO2的转化率为
| A.大于45.3% | B.小于45.3% | C.等于45.3% | D.无法确定 |
C
解析试题分析:催化剂只能加快反应速率,并不影响化学平衡,所以二氧化硫的转化率不变,答案选C。
考点:考查催化剂对化学平衡的影响

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
某温度下,在2L容器中3种物质间进行反应, X、Y、Z的物质的量随时间的变化曲线如图。下列叙述错误的是 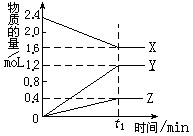
A.该反应的化学方程式是2X 3Y+Z 3Y+Z |
| B.在t1min时,该反应达到了平衡状态 |
| C.t1min时,X、Y、Z的反应速率相等 |
| D.当该反应已达到平衡状态时,每生成1molZ的同时生成2molX |
在一定温度下,10 mL 0.40mol/LH2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。下列叙述不正确的是(溶液体积变化忽略不计)
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
B.6~10 min的平均反应速率:v(H2O2)<3.3×10-2 mol/(L·min)
C.反应到6 min时,c(H2O2)=0.30mol/L
D.反应到6 min时,H2O2分解了50%
把镁带投入盛有盐酸的敞口容器里,下列因素对反应速率有影响的是
①盐酸的浓度 ②镁带的表面积 ③溶液的温度 ④氯离子的浓度
| A.①② | B.③④ | C.①②③④ | D.①②③ |
已知反应A2(g)+2B2 (g) 2AB2 (g)的ΔH<0,下列说法正确的是( )
2AB2 (g)的ΔH<0,下列说法正确的是( )
| A.升高温度,正向反应速率增加,逆向反应速率减小 |
| B.升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
| D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
下图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)
| A.等于1.369 g·L-1 |
| B.等于2.054 g·L-1 |
| C.在1.369g·L-1和2.054g·L-1之间 |
| D.在2.054g·L-1和4.108g·L-1之间 |
下列四支试管中,过氧化氢分解的化学反应速率最大的是
| 试管 | 温度 | 过氧化氢浓度 | 催化剂 |
| A | 室温(25℃) | 12% | 有 |
| B | 水浴加热(50℃) | 4% | 无 |
| C | 水浴加热(50℃) | 12% | 有 |
| D | 室温(25℃) | 4% | 无 |
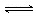 2C(g),可判断其达到化学平衡状态的是
2C(g),可判断其达到化学平衡状态的是