题目内容
一定条件下,反应2AB(g)?A2(g)+B2(g)达到平衡状态的标志是( )
| A、单位时间内生成n mol A2的同时消耗n mol B2 |
| B、容器内,AB、A2、B2三种气体共存 |
| C、AB的消耗速率等于A2的消耗速率 |
| D、容器中各组分的体积分数不随时间变化 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、单位时间内生成n mol A2等效于单位时间内生成n molB2 同时消耗n mol B2,正逆反应速率相等,故A正确;
B、容器内,AB、A2、B2三种气体共存,只要反应发生一直共存,故B错误;
C、AB的消耗速率等于A2的消耗速率,之比不等于计量数之比,故C错误;
D、容器中各组分的体积分数不随时间变化,说明达平衡状态,故D正确;故选AD.
B、容器内,AB、A2、B2三种气体共存,只要反应发生一直共存,故B错误;
C、AB的消耗速率等于A2的消耗速率,之比不等于计量数之比,故C错误;
D、容器中各组分的体积分数不随时间变化,说明达平衡状态,故D正确;故选AD.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
C5H12有3种不同结构:甲、CH3(CH2)3CH3,乙、CH3CH(CH3)CH2CH3 丙、C(CH3)4,下列相关叙述正确的是( )
| A、甲、乙、丙属同系物,均可与氯气、溴蒸气发生取代反应 |
| B、C5H12表示一种纯净物 |
| C、甲、乙、丙中,丙的沸点最低 |
| D、丙有3种不同沸点的二氯取代物 |
CPAE是蜂胶的主要活性成分,它可由咖啡酸合成,其合成过程如下.下列说法不正确的是( )


| A、1mol CPAE与足量的NaOH溶液反应,最多消耗3mol NaOH |
| B、可用金属Na检测上述反应是否残留苯乙醇 |
| C、与苯乙醇互为同分异构体的酚类物质共有9种 |
| D、咖啡酸可发生聚合反应,而且其分子中含有3种官能团 |
下列关于碳酸钠和碳酸氢钠的比较中,正确的是( )
| A、二者在水中的溶解度不同,碳酸氢钠的溶解度大于碳酸钠的溶解度 |
| B、二者热稳定性不同,碳酸钠的热稳定性大于碳酸氢钠的热稳定性 |
| C、二者都能与盐酸反应放出二氧化碳气体,但产气量和反应快慢不同 |
| D、二者在一定的条件下可以相互转化 |
有①氨水 ②NH4Cl溶液 ③Na2CO3溶液 ④NaHCO3溶液各25mL,物质的量浓度均为0.1mol/L,下列说法正确的是( )
| A、4种溶液pH的大小顺序:①>④>③>② |
| B、溶液①、②等体积混合后PH>7,则c(NH)<c(NH3?H2O) |
| C、向溶液①、②中分别加入25mL 0.1mol/L盐酸后,溶液中c(NH):①>② |
| D、向溶液③、④中分别加入12.5mL 0.1mol/L NaOH溶液后,前者c(HCO3-)<c(CO32-)后者c(HCO3-)>c(CO32-) |
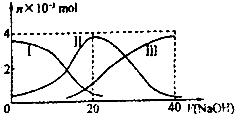 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量 变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量 变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).根据图示判断,下列说法正确的是( )| A、当V(NaOH)=20mL时,溶液中离子浓度大小关系 c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| B、等体积等浓度的NaOH溶液与H2A溶液混合后其溶液中水的电离程度比纯水大 |
| C、欲使NaHA溶液呈中性,可以向其中加入酸或碱 |
| D、向NaHA溶液加人水的过程中,pH可能增大也可能减小 |
X元素的阳离子和Y元素的阴离子具有相同的核外电子层结构.下列叙述中正确的是( )
| A、原子序数:X<Y |
| B、原子半径:X<Y |
| C、原子半径:X>Y |
| D、原子最外层电子数:X<Y |
为减少汽车尾气对大气造成的污染,目前市场上推出了使用乙醇汽油(在汽油中加入适量乙醇)的汽车.下列叙述错误的是( )
| A、乙醇汽油是一种化合物 |
| B、汽车使用乙醇汽油可以减少有害气体的排放 |
| C、乙醇充分燃烧生成CO2和H2O |
| D、用粮食发酵可制得乙醇 |