题目内容
1.下列化学反应的离子方程式正确的是( )| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 明矾溶于水产生Al(OH)3胶体:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
分析 A.次氯酸为弱酸,离子方程式中次氯酸不能拆开;
B.铝离子的水解为可逆反应,且氢氧化铝不能用沉淀符号;
C.醋酸为弱酸,离子方程式中醋酸不能拆开;
D.碳酸氢钠与足量的氢氧化钡反应生成碳酸钡沉淀、氢氧化钠和水.
解答 解:A.氯气溶于水生成硫化氢和次氯酸,正确的离子方程式为:Cl2+H2O═H++Cl-+HClO,故A错误;
B.明矾溶于水产生Al(OH)3胶体,正确的离子方程式为:Al3++3H2O?Al(OH)3+3H+,故B错误;
C.醋酸和碳酸钙都需要保留化学式,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故C错误;
D.碳酸氢钠溶液中加足量Ba(OH)2溶液,反应的离子方程式为:HCO3-+Ba2++OH-═BaCO3↓+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的正误判断,题目难度中等,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等,试题培养了学生灵活运用基础知识的能力.

练习册系列答案
相关题目
13.在含有下列离子的溶液中通入过量的SO2气体,这些离子仍可以大量共存的是( )
| A. | H+、Ca2+、Fe3+、NO3- | B. | Na+、CO32-、NH4+、Cl- | ||
| C. | Na+、K+、I-、OH- | D. | NH4+、K+、Cl-、SO42- |
12.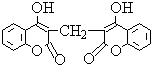 某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )
某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )
 某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )
某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )| A. | 有望将它发展制得一种抗凝血药 | |
| B. | 它无嗅并略具芳香味,因而可用来制备致命性出血型的杀鼠药 | |
| C. | 它可由化合物和甲醛(HCHO)通过缩合反应制得 | |
| D. | 它与足量NaOH溶液反应,消耗NaOH 6mol |
9.钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一.因而金属的防护工作特别重要.下列对几种常见金属防腐方法的描述错误的是( )
| 选项 | 方法 | 对相应方法的描述 |
| A | 改变金属内部的组成结构 | 此法实际上是将金属制成合金,增强抗腐蚀能力 |
| B | 在金属表面覆盖保护层 | 保护层破损后,就完全失去了对金属的保护作用 |
| C | 外加电流的阴极保护法 | 接外加直流电源构成电解池,被保护的金属作阴极 |
| D | 牺牲阳极的阴极保护法 | 构成原电池,被保护的金属作正极 |
| A. | A | B. | B | C. | C | D. | D |
6.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A. | 向AgCl悬浊液中加入稀的NaI溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B. | 在某溶液中加KSCN | 溶液显红色 | 该溶液中有Fe3+,无Fe2+ |
| C. | 在酒精灯上加热铝箔 | 铝箔熔化滴落下来 | 金属铝的熔点较低 |
| D. | 将气体通入澄清石灰水 | 溶液变浑浊 | 该气体一定是CO2 |
| A. | A | B. | B | C. | C | D. | D |
 按要求完成下列问题:
按要求完成下列问题: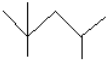 ;
; 或
或 .
.