题目内容
【题目】某学习小组设计以下四个实验探究氯水的成分,请根据下表回答问题。
实验序号 | 实验方法 | 实验现象 | 结论 |
① | 将氯水滴加到AgNO3溶液中 | 生成白色沉淀 | |
② | 将氯水滴加到含有酚酞的NaOH溶液中 | ||
③ | 淀粉KI试纸变蓝色 | 氯水中含有Cl2 | |
④ | 将足量的氯水滴加到Na2CO3溶液中 | 氯水中含有H+ |
(1)实验①得出的结论__________________________________________。
(2)指出实验②和实验④中的“实验现象”:②_____________;④____________。
(3)实验③中“实验方法”的具体操作过程是:___________________________________。
(4)通过实验②的“实验现象”,同学们得出两个不同的结论。这两个结论可能是a_____________,b._________。请设计简单的实验证明哪一个是正确的_______。
【答案】 氯水中含有Cl- 溶液褪色 有气泡冒出 取一片淀粉KI试纸,置于表面皿或玻璃片上,用洁净的玻璃棒蘸取氯水,滴在试纸上 氯水中含有HClO,其漂白作用使溶液褪色 氯水中含有H+,中和OH-使溶液褪色 向褪色后的溶液中滴加NaOH溶液至溶液显碱性,若溶液不再显红色,证明红色消失是HClO的漂白作用引起的;若溶液重新显红色,证明是H+的中和作用引起的
【解析】(1)加入硝酸银生成白色AgCl沉淀,可证明氯水中含有![]() ,因此,本题正确答案是:氯水中含有
,因此,本题正确答案是:氯水中含有![]() ;
;
(2)(2)氯水中含有盐酸,可与NaOH发生中和反应,含有次氯酸,具有强氧化性和漂白性,则可观察到溶液褪色;(4)氯水呈酸性,溶液中含有![]() ,加入
,加入![]() 溶液,生成二氧化碳气体,可观察到有气泡冒出,因此,本题正确答案是:溶液褪色;有气泡冒出;
溶液,生成二氧化碳气体,可观察到有气泡冒出,因此,本题正确答案是:溶液褪色;有气泡冒出;
(3)检验氯水中含有![]() ,可将氯水滴在淀粉
,可将氯水滴在淀粉![]() 试纸上没具体操作为取一小片KI淀粉试纸,置于表面皿或玻璃片上,用洁净的玻璃棒蘸取氯水,滴在试纸上,因此,本题正确答案是:取一小片KI淀粉试纸,置于表面皿或玻璃片上,用洁净的玻璃棒蘸取氯水,滴在试纸上;
试纸上没具体操作为取一小片KI淀粉试纸,置于表面皿或玻璃片上,用洁净的玻璃棒蘸取氯水,滴在试纸上,因此,本题正确答案是:取一小片KI淀粉试纸,置于表面皿或玻璃片上,用洁净的玻璃棒蘸取氯水,滴在试纸上;
(4)氯水中含有盐酸,可与NaOH发生中和反应,含有次氯酸,具有强氧化性和漂白性,都可使溶液褪色,则两种可能情况为:a为氯水加入到NaOH溶液中发生了中和反应而使溶液褪色,b为氯水中含有次氯酸就有漂白性而使溶液褪色,要验证结论的正误,可向褪色后的溶液中加NaOH溶液至碱性,溶液变红,可证明a正确,不再显红色,证明b正确,
因此,本题正确答案是:氯水加入到NaOH溶液中发生了中和反应而使溶液褪色;氯水中含有次氯酸就有漂白性而使溶液褪色;向褪色后的溶液中加NaOH溶液至碱性,溶液变红,可证明a正确,不再显红色,证明b正确;

 名校课堂系列答案
名校课堂系列答案【题目】已知25℃时,几种酸的电离平衡常数如下表所示。
序号 | ① | ② | ③ | ④ |
酸 | HF | CH3COOH | H2SeO4 | H2CO3 |
Ka1 | 6.4×10-4 | 1.8×10-5 | 完全电离 | 4.4×10-7 |
Ka2 | 1.0×10-2 | 4.7×10-11 |
(1)25℃时,pH=3 的盐酸V1mL与pH= 12 的氢氧化钠溶液V2mL混合后恰好成中性,则V1:V2=____:___。
(2)25℃时,0.1mol·L-1 HF 溶液的 c(H+)约为______mol·L-1 。将pH均3 的①、②、③溶液分别加水稀释至原来的10 倍,溶液的pH 大小关系:_____ (填序号)。
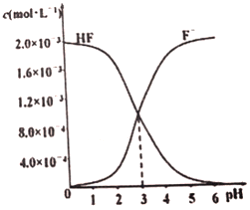
(3)在T℃时调节2.0×10-3mol·L-1 的氢氟酸水溶液的pH(忽略调节时体积变化),测得平衡体系中c(F-)、c(HF)与溶液pH 的关系如图所示。则HF 电离平衡常数为Ka(HF)=_________。
(4)向H2SeO4 溶液中滴加少量氨水,反应的离子方程式为___________________________。若将一定浓度的KHCO3 和KHSeO4两溶液混合,反应的离子方程式为_________________________。