题目内容
已知元素A、B、C、D和E的原子序数依次增大。A、B、C、D四种元素核电荷数均小于20,A、B同主族;B、C、D元素的基态原子具有相同的能层数,它们的基态原子中p能级上未成对电子数分别为1、3、1;E是周期表中(除放射性元素外)第一电离能最小的元素。回答下列问题:
(1)写出下列元素的符号:A 、E 。
(2)C元素的价电子排布图为: ;
该排布遵循的原理主要有: (答完整得分)。
(3)C、D元素形成的化合物主要有: (填化学式,答完整得分);其中相对分子质量较小的分子为 分子(填“极性”或“非极性”),该分子的空间构型为 ,中心原子的杂化方式是 。
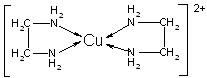
(4)化合物BD3的熔点190℃、沸点182.7℃,那么BD3的晶体类型为 ;事实上,在BD3的化合物中往往以B2D6的形式存在,该形式的存在是由于 形成的。(选填“氢键”、“范德华力”、“离子键”、“配位键”)
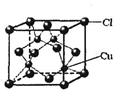
(5)下图为几种晶胞(或晶胞的1/8)示意图,其中 和
和 代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。
代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。
(1)写出下列元素的符号:A 、E 。
(2)C元素的价电子排布图为: ;
该排布遵循的原理主要有: (答完整得分)。
(3)C、D元素形成的化合物主要有: (填化学式,答完整得分);其中相对分子质量较小的分子为 分子(填“极性”或“非极性”),该分子的空间构型为 ,中心原子的杂化方式是 。
(4)化合物BD3的熔点190℃、沸点182.7℃,那么BD3的晶体类型为 ;事实上,在BD3的化合物中往往以B2D6的形式存在,该形式的存在是由于 形成的。(选填“氢键”、“范德华力”、“离子键”、“配位键”)
(5)下图为几种晶胞(或晶胞的1/8)示意图,其中
 和
和 代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。
代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。
(1)B Cs (2)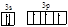 构造原理、泡利原理、洪特规则
构造原理、泡利原理、洪特规则
(3)PCl3、PCl5 极性 三角锥形 sp3
(4)分子晶体 配位键 (5)B 8
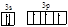 构造原理、泡利原理、洪特规则
构造原理、泡利原理、洪特规则(3)PCl3、PCl5 极性 三角锥形 sp3
(4)分子晶体 配位键 (5)B 8
试题分析:(1)B、C、D元素的基态原子具有相同的能层数,它们的基态原子中p能级上未成对电子数分别为1、3、1,且原子序数依次递增,都小于20,所以B是硼或铝元素,由于A和B是同主族的,且A的原子序数最小,所以B是Al,A是B,则C是P,D是Cl。E是周期表中(除放射性元素外)第一电离能最小的元素,由于金属性越强,第一电离能越小,所以E是Cs。
(2)根据构造原理可知,P元素的价电子排布图为
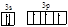 ,该排布图除了遵循构造原理外,还遵循了泡利原理、洪特规则。
,该排布图除了遵循构造原理外,还遵循了泡利原理、洪特规则。(3)P和Cl形成的化合物有PCl3、PCl5。其中相对分子质量较小的PCl3,由于P原子含有1对孤对电子,所以是三角锥形结构,属于极性分子,而中心原子P原子是sp3杂化。
(4)根据氯化铝的熔沸点较低可知,该化合物形成的晶体应该是分子晶体。由于氯元素含有孤对电子,而铝元素含有空轨道,所以还可以形成配位键。
(5)氯化铯形成的晶体是离子晶体,晶体中配位数是8,所以答案选B。
点评:该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。

练习册系列答案
相关题目

 若
若 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)