��Ŀ����
����Ŀ��ˮ���������Ǵ������������Ҫ�ɷ�,�о��仯ѧ��ɶ�������������Ⱦ�����ش����壬ij�������������ᆳ�������Ҫ��Ԥ�������������Һ��������ɫ����ȷ��������������NH4+��Na+��Mg2+��Ca2+��Al3+��SO42-��NO3-��CO32-��Cl-��ijͬѧ�����ٽ������µ�ʵ��:
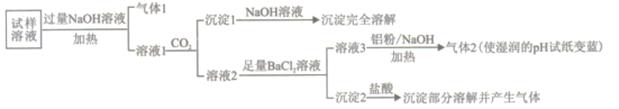
��֪���ڼ�����ǿ����������,�����ʿ��Խ�NO3-��ԭΪ������
�ش���������:
��1��������1���ĵ���ʽΪ_________��
��2������������1�������ӷ���ʽΪ________��
��3��������2���ijɷ���___________(�ѧʽ)��
��4������Һ3![]() ����2�������ӷ���ʽΪ_________��
����2�������ӷ���ʽΪ_________��
��5����������ʵ����ƶϸõ���������������__________�����ϵ�(�����ӷ���)��
��6����֪�����������и�Ԫ�ص���Ⱦ�������±�:
Ԫ�� | N | S | Na��Mg��Cl | Al | Ca |
��Ⱦ���� | ������β�� | ȼú��Ⱦ | �������� | �����ﳾ | �����۳� |
����ʵ�������жϸõ���������������Ⱦ������___________��
���𰸡� ![]() [Al(OH)4]-+CO2=A l(OH)3��+HCO3- BaSO4��BaCO3 8Al+3NO3-+5OH-+18H2O
[Al(OH)4]-+CO2=A l(OH)3��+HCO3- BaSO4��BaCO3 8Al+3NO3-+5OH-+18H2O ![]() 3NH3��+8[Al(OH)4]- Mg2+��Ca2+��CO32- ������β����ȼú��Ⱦ�������ﳾ
3NH3��+8[Al(OH)4]- Mg2+��Ca2+��CO32- ������β����ȼú��Ⱦ�������ﳾ
����������1������֪��������Һ�е�NH4+�����NaOH��Һ��Ӧ�����Ȳ���������1Ϊ����(NH3)���ʵ���ʽΪ��![]() ��
��
��2��������Һ�е�Al3+�����NaOH��Һ��Ӧ����[Al(OH)4]-��[Al(OH)4]-��CO2��Ӧ����Al(OH)3������Al(OH)3������NaOH��Һ��Ӧ����[Al(OH)4]-�������ܽ⣬���Գ���1ΪAl(OH)3������������1�������ӷ���ʽΪ��[Al(OH)4]-+CO2=Al(OH)3��+HCO3-��
��3�������̣�����2�м����ᣬ���������ܽⲢ�������壬�����֪������ɫ�������ɵã�����2ӦΪBaSO4��BaCO3�Ļ���
��4�������У���Һ3�������ۺ�NaOH�����������ɵ�����2��ʹʪ���pH��ֽ������������2Ϊ����������֪���ڼ�����ǿ�����������������ʿ��Խ�NO3-��ԭΪ��������������Һ3![]() ����2�������ӷ���ʽΪ��8Al+3NO3-+5OH-+18H2O
����2�������ӷ���ʽΪ��8Al+3NO3-+5OH-+18H2O![]() 3NH3��+8[A1(OH)4]-��
3NH3��+8[A1(OH)4]-��
��5������������Һ�ӹ���NaOH��Һû�в����������ɵ�Mg2+�����ϵͣ����ݳ���1��ȫ�ܽ���NaOH��Һ���ɵó���1��û��CaCO3��Ca2+��CO32-�����ϵͣ����Ը�������ʵ����ƶϸõ���������������Mg2+��Ca2+��CO32-�����ϵ���
��6������ʵ�������жϸõ���������������Mg2+��Ca2+��CO32-�����ϵͣ���ϱ����ṩ����Ϣ�ɵã�������β����ȼú��Ⱦ�������ﳾ�Ǹõ���������������Ⱦ������