题目内容
将3 mol A和2.5 mol B混合于2L的密闭容器中,发生反应的化学方程式为:3A(气) + B(气) 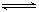 xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 填写下列空白:
xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 填写下列空白:
(1) x =______
(2) 平衡时C的浓度为 ________________
(3) 平衡时B的转化率为 _____________
(4) 平衡时,容器内的压强与原容器内压强的比值为 ___________
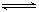 xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 填写下列空白:
xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 填写下列空白:(1) x =______
(2) 平衡时C的浓度为 ________________
(3) 平衡时B的转化率为 _____________
(4) 平衡时,容器内的压强与原容器内压强的比值为 ___________
(1)X="1" (2) 0.25mol·L-1 (3)20% (4)10∶11
容器内的压强变小,说明3+1>x+2,又因为x是整数,所以x=1。D的平均反应速度为 0.1 mol/(L﹒min),,则生成D是0.1 mol/(L﹒min),×2L×5min=1.0mol
3A(气) + B(气)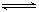 C(气) + 2D(气)
C(气) + 2D(气)
起始量(mol) 3 2.5 0 0
转化量(mol) 1.5 0.5 0.5 1.0
平衡量(mol) 1.5 2.0 0.5 1.0
所以平衡时C的浓度为0.5mol÷2L=0.25mol/L
平衡时B的转化率为0.5÷2.5×100%=20%
因为压强之比是物质的量的之比
所以平衡时,容器内的压强与原容器内压强的比值为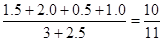
3A(气) + B(气)
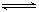 C(气) + 2D(气)
C(气) + 2D(气)起始量(mol) 3 2.5 0 0
转化量(mol) 1.5 0.5 0.5 1.0
平衡量(mol) 1.5 2.0 0.5 1.0
所以平衡时C的浓度为0.5mol÷2L=0.25mol/L
平衡时B的转化率为0.5÷2.5×100%=20%
因为压强之比是物质的量的之比
所以平衡时,容器内的压强与原容器内压强的比值为
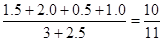

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
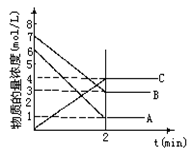
 4C
4C ,达到平衡时,C的物质的量百分含量为w,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的物质的量百分含量大于w的是
,达到平衡时,C的物质的量百分含量为w,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的物质的量百分含量大于w的是
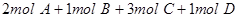
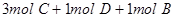
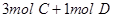
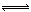 CO2(aq),CO2(aq)+H2O
CO2(aq),CO2(aq)+H2O 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( )  2HI(g),下列情况一定能说明反应已达到平衡状态的是( )
2HI(g),下列情况一定能说明反应已达到平衡状态的是( ) 2NH3(正反应为放热反应)达到平衡后,下列选项中三种方法都能使平衡向正反应方向移动的是( )
2NH3(正反应为放热反应)达到平衡后,下列选项中三种方法都能使平衡向正反应方向移动的是( )