题目内容
【题目】决定物质性质的重要因素是物质结构.请回答下列问题. 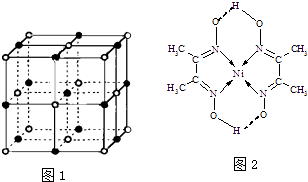
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
电离能/kJmol﹣1 | I1 | I2 | I3 | I4 |
A | 578 | 1817 | 2745 | 11578 |
B | 738 | 1451 | 7733 | 10540 |
A通常显价,B元素的核外电子排布式为 .
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示),已知3种离子晶体的晶格能数据如表:
离子晶体 | NaCl | KCl | CaO |
晶格能/kJmol﹣1 | 786 | 715 | 3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是 . 其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有个.
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是 .
(4)某配合物的分子结构如图2所示,其分子内不含有(填序号).
A.离子键
B.极性键
C.金属键
D.配位键
E.氢键
F.非极性键.
【答案】
(1)+3;1s22s22p63s2
(2)TiN>MgO>CaO>KCl;12
(3)CrO2
(4)AC
【解析】解:(1)A的I4电离能突然增大,说明最外层有3个电子,应为Al,B的I3电离能突然增大,说明最外层有2个电子,应为Mg,Al的正化合价为+3价,Mg的核外有12个电子,分三层排布,其电子排布式为:1s22s22p63s2;所以答案是:+3;1s22s22p63s2;(2)离子晶体中晶格能越大,形成的离子晶体越稳定,熔点越高硬度越大,晶格能与离子的半径、电荷有关,电荷越多、离子半径越小,晶格能越大,TiN中阴阳离子所带电荷为3,大于其它离子所带电荷,MgO、CaO中所带电荷相同,但镁离子半径小于钙离子半径,氯化钾中阴阳离子所带电荷为1,且钾离子半径>钙离子半径,氯离子半径大于氧离子半径,所以KCl、MgO、CaO、TiN4种离子晶体熔点从高到低的顺序是TiN>MgO>CaO>KCl; MgO的晶体结构与NaCl的晶体结构相似,所以一个Mg2+周围和它最邻近且等距离的Mg2+个数为12.所以答案是:TiN>MgO>CaO>KCl;12;(3)V2O5中V的最外层电子全部失去或成键,CrO2中Cr失去4个电子,离子的最外层电子为2,为成对,离子含未成对电子越多,则磁性越大,则适合作录音带磁粉原料的是CrO2 , 所以答案是:CrO2;(4)该配合物中存在的化学键有:非金属元素之间的共价键,镍元素与氮元素之间的配位键,氧原子和氢原子之间的氢键,故选AC.所以答案是:AC.

【题目】二氧化碳是全球气候变化的主要罪魁祸首,为消除二氧化碳的污染并使其转变为有用物质,全世界的化学科学家做了大量的研究.科学家找到了一种名叫二硒化钨的金属化合物,通过处理,在阳光作用下,使二氧化碳较易分解成一氧化碳和氧气,用一氧化碳可轻松获得多种能源物质.如CO和H2可以合成甲醇.
在10L的密闭容器中按物质的量之比1:2充入CO和H2 , 若充有10molCO发生反应:CO(g)+2H2(g)CH3OH(g).
测得平衡时CO的转化率隨温度变化及压强的变化如图所示:
p2、T2时,n(CO)随时间的变化如表所示:
t/min | 0 | 1 | 3 | 5 |
n(CO)/mol | 10 | 7 | 5 | 5 |
(1)p2、T2时,0~lmin 内,平均速率ν(H2)=mol/(Lmin);
(2)你认为p1p2(填“<”“>”或“=”)
(3)合成甲醇的反应为(填“放热”或“吸热”)反应.A、B、C三点的平衡常数KA、KB、KC的大小关系为 .
(4)若工业生产CH3OH,下列措施中,能增加单位时间内CH3OH产量的方法有 .
①增大压强 ②降低温度 ③升高温度
④加入催化剂 ⑤适当增大一氧化碳的比例量 ⑥及时分离CH3OH
(5)己知碳的燃烧热为Q1kJ/mol,碳与氧气反应生成一氧化碳(按量筒整数比)的反应热为﹣Q2J/mol,则二氧化碳在二硒化钨作催化剂时分解的热化学方程式(按最简整数比)为: .
【题目】下列检验方法与结论相符的一组是( )
序号 | 检 验 方 法 | 结 论 |
A | 向一种未知溶液中滴加AgNO3溶液,有白色沉淀 | 未知溶液中一定含有Cl﹣ |
B | 向一种未知溶液中滴加盐酸,有气泡产生 | 未知溶液中一定含有CO |
C | 将一种未知气体通入品红溶液,溶液褪色,加热后又恢复红色 | 未知气体是SO2 |
D | 向一种未知溶液中滴加BaCl2溶液,有白色沉淀 | 未知溶液中一定含有SO |
A.A
B.B
C.C
D.D

