题目内容
【题目】无机化合物可根据其组成和性质进行分类:
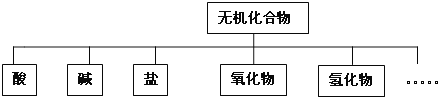
(1)上述所示的物质分类方法名称是 ______ .
(2)①CO2 ②Cu ③FeCl3溶液 ④H2SO4 ⑤氢氧化铁体胶体 ⑥Al2(SO4)3固体 ⑦酒精 ⑧BaSO4固体
属于电解质的是 ______ ;属于非电解质的是 ______ (填序号)。
(3)请写出⑥的电离方程式______________________________________________
(4)下列关于③和⑤的说法正确的是____________。
a.都不稳定,密封静置会产生沉淀
b.⑤能产生丁达尔效应,而③不能
c.加入盐酸都会产生沉淀
(5)按要求写出下列反应的离子方程式:
①锌跟稀硫酸反应_________________________________________________。
②氢氧化钡溶液和稀硫酸反应 ______________________________________。
③MgO滴加稀盐酸_______________________________________________。
【答案】树状分类法 ④⑥⑧ ①⑦ Al2(SO4)3 = 2Al3+ + 3SO42- b Zn+2H+=Zn2++H2↑ Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O MgO+2H+=Mg2++H2O
【解析】
(1)上述所示的物质分类方法名称是树状分类法;
(2)①二氧化碳为酸性氧化物、⑦酒精为一般的有机物,均为非电解质;
②Cu为单质、③FeCl3溶液为混合物、⑤氢氧化铁体胶体为混合物,既不属于电解质也不属于非电解质;
④H2SO4为酸、⑥Al2(SO4)3固体为盐、⑧BaSO4固体为盐,均为电解质;
故电解质为④⑥⑧,非电解质为①⑦;
(3)Al2(SO4)3固体的电离方程式为Al2(SO4)3 = 2Al3+ + 3SO42-;
(4)a. ③为溶液,较稳定,静置后不会产生沉淀,a错误;
b. ⑤为胶体、③为溶液,⑤能产生丁达尔效应,而③不能,b正确;
c. FeCl3溶液加入盐酸无明显现象,c错误;
故答案选b;
(5)①锌跟稀硫酸反应的方程式为Zn+2H+=Zn2++H2↑
②氢氧化钡溶液和稀硫酸反应的方程式为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
③MgO滴加稀盐酸反应的方程式为MgO+2H+=Mg2++H2O
注意②中不要局部约分,③中MgO为难溶物不要拆成离子形式。

 口算能手系列答案
口算能手系列答案【题目】下述实验操作中,正确的是( )
|
|
|
|
A.配制硫酸溶液时,将浓硫酸慢慢注入盛有水的容量瓶中进行配制 | B.用托盘天平称量药品时,将药品置于天平左盘 | C.将混合液蒸馏分离时,应使温度计水银球浸没在混合液中 | D.分液时,将上下层液体依次从分液漏斗下口分别流入两个烧杯中 |
A.AB.BC.CD.D
【题目】某工业废水仅含下表中的某些离子,且各种离子的物质的量浓度相等,均为0.1 mol/L(此数值忽略水的电离及离子的水解)。
阳离子 | K+ Ag+ Mg2+ Cu2+ Al3+ NH4+ |
阴离子 | Cl- CO32— NO3— SO42— SiO32— I- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取该无色溶液5 mL,滴加一滴氨水有沉淀生成,且离子种类增加。
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰。
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是____________。
(2)Ⅲ中加入盐酸生成无色气体的离子方程式是_____________________________。
(3)甲同学最终确定原溶液中所含阳离子有________,阴离子有________;并据此推测原溶液应该呈_______________________________________________性,原因是_________________________________(请用离子方程式说明)。
(4)另取100 mL原溶液,加入足量的NaOH溶液,此过程中涉及的离子方程式为__________________________________________________________。充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体质量为________g。