题目内容
已知:CH4(g)+2O2(g)==CO2(g)+2H2O(1) △H1 = ―Q1 KJ/mol
2H2(g)+O2(g)==2H2O(g) △H2= ―Q2 KJ/mol
2H2(g)+O2(g)==2H2O(1) △H3 = ―Q3KJ/mol
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则下列说法正确的是( )
2H2(g)+O2(g)==2H2O(g) △H2= ―Q2 KJ/mol
2H2(g)+O2(g)==2H2O(1) △H3 = ―Q3KJ/mol
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则下列说法正确的是( )
| A.放出的热量为(0.4Q1+0.05Q3)KJ | B.放出的热量为(0.4Q1+0.05Q2)KJ |
| C.△H2 = △H3 | D.△H2 <△H3 |
A
标准状况下11.2L气体是0.5mol,其中甲烷是0.4mol,氢气是0.1molo,燃烧后恢复至室温时水是液态,所以最终放出的热量是(0.4Q1+0.05Q3)KJ。气态水的能量高于液态水的能量,所以氢气燃烧生成液态水放出的能量多,放热越多,反应热越小。所以答案选A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 2NH3(g) +
2NH3(g) + 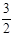 O2(g) ;△H =" a" kJ·mol—1
O2(g) ;△H =" a" kJ·mol—1 2H2O(l) ΔH = -571.6kJ·mol—1
2H2O(l) ΔH = -571.6kJ·mol—1

 2NH3(g)能量变化如右图,回答下列问题:
2NH3(g)能量变化如右图,回答下列问题: