题目内容
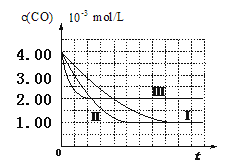
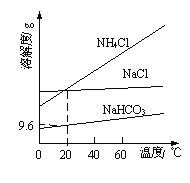
【题目】以NaCl、CO2、NH3为原料发生反应,制得NaHCO3和NH4Cl是“侯氏制碱法”的重要步骤。相关物质的溶解度曲线如图所示。下列说法不正确的是
A.将NaHCO3加热分解可得纯碱
B.常温下碳酸氢钠的溶解度大于碳酸钠
C.采用蒸发结晶从溶液中分离出NaHCO3
D.20℃时,NaHCO3饱和溶液的物质的量浓度约为1.1mol/L
【答案】BC
【解析】
试题分析:A.碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,将NaHCO3加热分解可得纯碱,故A正确;B.Na2CO3+CO2+H2O=2NaHCO3↓,常温下碳酸氢钠溶解度小于碳酸钠,故B错误;
C.碳酸氢钠受热分解,采用蒸发结晶不能从溶液中分离出NaHCO3,故C错误;D.20℃时碳酸氢钠溶解度为9.6g,溶质物质的量n=![]() =
=![]() =0.114mol,溶液体积近似为100ml计算得到c=
=0.114mol,溶液体积近似为100ml计算得到c=![]() =1.1mol/L,故D正确。故选BC。
=1.1mol/L,故D正确。故选BC。

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目