题目内容
【题目】关于下列图示的说法中不正确的是

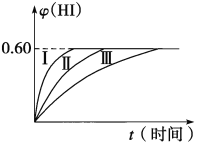
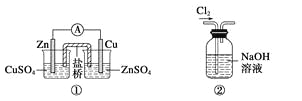
A.图①表示CO(g)+H2O(g)![]() CO2(g)+H2(g)是放热反应
CO2(g)+H2(g)是放热反应
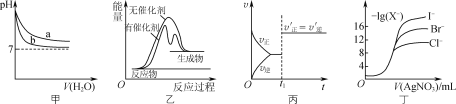
B.图②为电解硫酸铜溶液的装置,电解一段时间后,加入一定量的Cu(OH)2一定不能使溶液恢复到电解前的浓度和体积
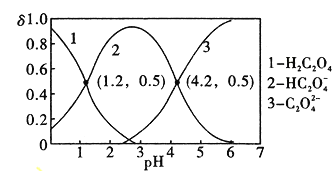
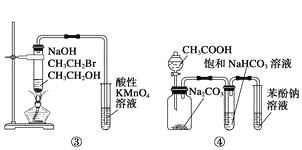
C.图③实验装置可一次而又科学准确的完成比较HCl、H2CO3、H2SiO3酸性强弱的实验
D.图④两个装置中通过导线的电子数相同时,正极生成气体的物质的量也相同
【答案】BC
【解析】
A、图中反应物总能量高于生成物总能量,CO(g)+H2O(g)![]() CO2(g)+H2(g)是放热反应,A正确;
CO2(g)+H2(g)是放热反应,A正确;
B、石墨电极电解硫酸铜溶液,阳极是氢氧根离子放电产生氧气,阴极是铜离子放电,析出铜,铜离子放电完毕后溶液中的氢离子放电产生氢气,因此电解一段时间后,加入一定量的Cu(OH)2可能使溶液恢复到电解前的浓度和体积,B错误;
C、由于盐酸易挥发,生成的二氧化碳中含有氯化氢,HCl与硅酸钠溶液反应也产生白色沉淀,因此不能比较碳酸和硅酸的酸性强弱,C错误;
D、两个装置中正极均是溶液中的氢离子放电产生氢气,所以两个装置中通过导线的电子数相同时,正极生成气体的物质的量也相同,D正确;
答案选BC。

练习册系列答案
相关题目