题目内容
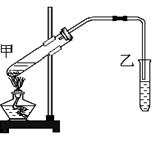
(6分)图5是实验室制取Cl2并以Cl2为原料进行特定反应的实验:
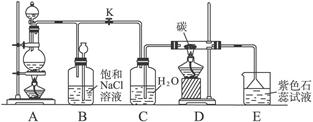
图5
(1)A为氯气发生装置,写出反应的化学方程式:_________________________________。
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯,连上E装置。Cl2通过C瓶后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl(g),试写出D装置中反应的化学方程式_______________________;装置C的作用是_________________________________。
(3)E处石蕊试液的现象是_____________________________________________________,其原因是______________________________________________________________________。
(4)若将E处溶液改为石灰水,反应过程的现象是_________________________________。
a.有白色沉淀生成
b.无白色沉淀生成
c.先生成白色沉淀,然后沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是________________________,B的作用是
___________________________。

图5
(1)A为氯气发生装置,写出反应的化学方程式:_________________________________。
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯,连上E装置。Cl2通过C瓶后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl(g),试写出D装置中反应的化学方程式_______________________;装置C的作用是_________________________________。
(3)E处石蕊试液的现象是_____________________________________________________,其原因是______________________________________________________________________。
(4)若将E处溶液改为石灰水,反应过程的现象是_________________________________。
a.有白色沉淀生成
b.无白色沉淀生成
c.先生成白色沉淀,然后沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是________________________,B的作用是
___________________________。
(1)MnO2+4HCl(浓)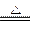 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)2Cl2+C+2H2O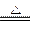 4HCl+CO2 提供D处所需的水蒸气
4HCl+CO2 提供D处所需的水蒸气
(3)石蕊试液先变红色,后变无色 生成的HCl使石蕊试液变红,未反应完的Cl2与H2O作用产生HClO,HClO的漂白作用使红色消失
(4)b
(5)B瓶中液面下降,同时长颈漏斗内液面上升 贮存少量Cl2,避免Cl2对环境的污染
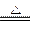 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(2)2Cl2+C+2H2O
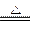 4HCl+CO2 提供D处所需的水蒸气
4HCl+CO2 提供D处所需的水蒸气(3)石蕊试液先变红色,后变无色 生成的HCl使石蕊试液变红,未反应完的Cl2与H2O作用产生HClO,HClO的漂白作用使红色消失
(4)b
(5)B瓶中液面下降,同时长颈漏斗内液面上升 贮存少量Cl2,避免Cl2对环境的污染
实验室中制取Cl2常用MnO2与浓盐酸在加热条件下反应,反应原理:MnO2+4HCl(浓)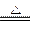 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)从生成物CO2和HCl(g)可以推理H2O与Cl2、C同时参与反应,其反应方程式为:2Cl2+C+2H2O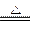 4HCl+CO2。装置C的作用是提供D处所需的水蒸气。
4HCl+CO2。装置C的作用是提供D处所需的水蒸气。
(3)石蕊试液先变红色,后变无色;生成的HCl使石蕊试液变红。未反应完的Cl2与H2O作用产生HClO,HClO的漂白作用使红色消失。
(4)从(2)反应不难分析,CO2和HCl同时作用于石灰水,且HCl与CO2的体积比为4∶1,显然盐酸过量,不能生成CaCO3沉淀。故答案为b。
(5)少量Cl2进入B瓶,由于瓶内压强增大, B瓶中液面下降,同时长颈漏斗内液面上升;B的作用是贮存少量Cl2,避免Cl2对环境的污染。
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(2)从生成物CO2和HCl(g)可以推理H2O与Cl2、C同时参与反应,其反应方程式为:2Cl2+C+2H2O
 4HCl+CO2。装置C的作用是提供D处所需的水蒸气。
4HCl+CO2。装置C的作用是提供D处所需的水蒸气。(3)石蕊试液先变红色,后变无色;生成的HCl使石蕊试液变红。未反应完的Cl2与H2O作用产生HClO,HClO的漂白作用使红色消失。
(4)从(2)反应不难分析,CO2和HCl同时作用于石灰水,且HCl与CO2的体积比为4∶1,显然盐酸过量,不能生成CaCO3沉淀。故答案为b。
(5)少量Cl2进入B瓶,由于瓶内压强增大, B瓶中液面下降,同时长颈漏斗内液面上升;B的作用是贮存少量Cl2,避免Cl2对环境的污染。

练习册系列答案
相关题目
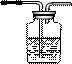
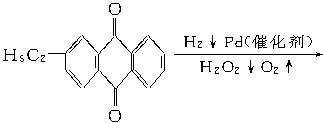
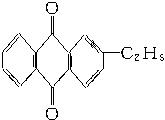

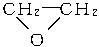 +CaCl2+H2O,则制备
+CaCl2+H2O,则制备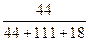 ×100%。在绿色化学工艺中,原子的利用率为100%的工艺称理想状态的“绿色工艺”。本题提供的生成H2O2的方法,可否称为理想状态的“绿色工艺”?简述理由。
×100%。在绿色化学工艺中,原子的利用率为100%的工艺称理想状态的“绿色工艺”。本题提供的生成H2O2的方法,可否称为理想状态的“绿色工艺”?简述理由。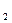 +4HCl(浓)
+4HCl(浓) MnCl
MnCl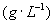 分别表示溶质在A、B两种溶剂中的浓度,则有c(A)/c(B)=K。对于
分别表示溶质在A、B两种溶剂中的浓度,则有c(A)/c(B)=K。对于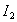 而言,
而言, 。现有2.0L碘水,其中含
。现有2.0L碘水,其中含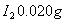 ,若用
,若用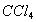 萃取,按两种方法萃取:第一种方法用50mL
萃取,按两种方法萃取:第一种方法用50mL