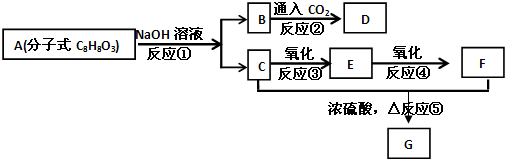
题目内容
有下列6种物质①氯水 ②酒精 ③熔融Al2O3 ④石墨 ⑤纯碱 ⑥钢(填标号)
能导电的是: 属于混合物的是: 属于非电解质的是: 属于电解质的是: .
能导电的是:
考点:混合物和纯净物,电解质与非电解质,电解质溶液的导电性
专题:电离平衡与溶液的pH专题
分析:据物质导电的原因分析,只要含有自由移动的离子或自由电子即可;
纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质;
电解质在水溶液里或熔融状态下能导电的化合物是电解质,前提必须是化合物;
非电解质是在水溶液里或熔融状态下都不能导电的化合物,前提必须是化合物.
纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质;
电解质在水溶液里或熔融状态下能导电的化合物是电解质,前提必须是化合物;
非电解质是在水溶液里或熔融状态下都不能导电的化合物,前提必须是化合物.
解答:
解:①氯水③熔融Al2O3中有自由移动的离子,所以能导电;④石墨 ⑥钢有自由电子,所以能导电;
①氯水是氯气的水溶液,属于混合物;⑥钢是铁和碳形成的合金,属于混合物;
非电解质是在水溶液里或熔融状态下都不能导电的化合物,②酒精属于非电解质;
在水溶液里或熔融状态下能导电的化合物是电解质,所以③熔融Al2O3 ⑤纯碱是电解质;
故答案为:①③④⑥;①⑥;②;③⑤.
①氯水是氯气的水溶液,属于混合物;⑥钢是铁和碳形成的合金,属于混合物;
非电解质是在水溶液里或熔融状态下都不能导电的化合物,②酒精属于非电解质;
在水溶液里或熔融状态下能导电的化合物是电解质,所以③熔融Al2O3 ⑤纯碱是电解质;
故答案为:①③④⑥;①⑥;②;③⑤.
点评:本题考查了电解质溶液导电的原因及电解质、非电解质、弱电解质的定义,能导电的不一定是电解质,电解质不一定能导电.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
对于化合物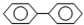 ,下列叙述中正确的是( )
,下列叙述中正确的是( )
 ,下列叙述中正确的是( )
,下列叙述中正确的是( )| A、其化学式为C12H12 |
| B、分子中所有原子有可能处于同一平面 |
| C、该化合物分子中所有原子不可能处于同一平面 |
| D、分子中所有原子一定处于同一平面 |
下列物质的化学用语不正确的是( )
| A、乙酸乙酯的最简式:C2H4O |
B、乙烯的比例模型: |
C、甲烷分子的球棍模型: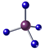 |
| D、乙烷的结构式:CH3CH3 |
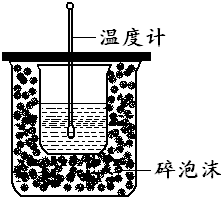 在如图所示的装置中进行中和反应的反应热测定,实验操作如下:
在如图所示的装置中进行中和反应的反应热测定,实验操作如下: