题目内容
【题目】已知:—CHO+ +H2O,由于醚键比较稳定故利用此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )
+H2O,由于醚键比较稳定故利用此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )
A.保护1mol醛基时也可用![]()
B.合成1mol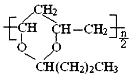 需要1mol
需要1mol![]() 和
和![]()
C.通过上述反应合成的![]() 其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3
其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3
D.![]() 可由
可由![]() 与
与![]() 通过上述反应得到
通过上述反应得到
【答案】B
【解析】
A.由题给信息可知1mol醛基可与2mol羟基反应;
B. 由CH2=CHOH与CH3CH2CH2CHO生成;
由CH2=CHOH与CH3CH2CH2CHO生成;
C.![]() 结构不对称,含有8种H;
结构不对称,含有8种H;
D.由信息可知![]() 对应的反应物之一应含有4个-OH。
对应的反应物之一应含有4个-OH。
A.由题给信息可知1mol醛基可与2mol羟基反应,则保护1mol醛基时也可用2molCH3CH2OH,故A正确;
B. 对应的单体含有C=C键,由nmolCH2=CHOH与0.5nmolCH3CH2CH2CHO生成,故B错误;
对应的单体含有C=C键,由nmolCH2=CHOH与0.5nmolCH3CH2CH2CHO生成,故B错误;
C.![]() 结构不对称,含有8种H,且核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3,故C正确;
结构不对称,含有8种H,且核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3,故C正确;
D.由信息可知![]() 对应的反应物之一应含有4个-OH,为C(CH2OH)4与
对应的反应物之一应含有4个-OH,为C(CH2OH)4与![]() ,故D正确。
,故D正确。
故选:B。

【题目】按要求回答下列问题
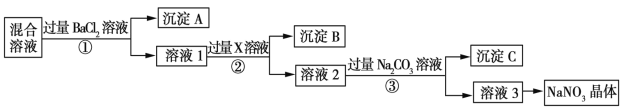
(1)我国规定生活用水中镉排放的最大允许浓度为0.005 mg/L。处理含镉废水可采用化学沉淀法。试回答下列问题:
①磷酸镉(Cd3(PO4)2)沉淀溶解平衡常数的表达式Ksp=_____________________。
②在某含镉废水中加人Na2S,当S2-浓度达到7.9 × 10-8mol/L时,水体中Cd2+浓度为_____mol/L(已知:Ksp(CdS)=7.9 × 10-27,Cd的相对原子质量:112);此时是否符合水源标准?______(填“是”或“否”)。
(2)炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。制取氯化锌主要工艺如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
金属离子 | Fe3+ | Zn2+ | Fe2+ |
开始沉淀的pH | 1. 1 | 5. 2 | 5. 8 |
沉淀完全的pH | 3. 2 | 6. 4 | 8. 8 |
①加入H2O2溶液的作用是________________。
②流程图中,调节pH时,加入的试剂X可以是________(填序号);
a、ZnO b、NaOH c、Zn2(OH)2CO3 d、ZnSO4
pH应调整到______________________。