题目内容
【题目】室温下,下列事实不能说明NH3H2O为弱电解质的是( )
A.相同浓度下的NH3H2O 溶液中含有的OH﹣浓度小于 NaOH
B.相同条件下,浓度均为0.1molL﹣1NaOH溶液和氨水,氨水的导电能力弱
C.0.1molL﹣1NH3H2O能使无色酚酞试液变红色
D.OH﹣浓度相同的NH3H2O 和 NaOH 溶液分别加水稀释,c(OH﹣)随溶液体积变化的曲线如图所示,其中曲线Ⅱ是 NH3H2O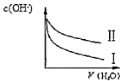
【答案】C
【解析】
抓住弱电解质的本质不完全电离及电离平衡进行突破。
A.同为一元碱且浓度相同,NaOH为强碱,完全电离,NH3H2O 溶液中含有的OH﹣浓度小于 NaOH,说明NH3H2O不完全电离,A项正确;
B.电解质溶液的导电能力与离子浓度有关,同浓度NaOH溶液和氨水,氨水的导电能力弱,反映离子浓度小,说明NH3H2O不完全电离,B项正确;
C. NH3H2O使无色酚酞试液变红色可以说明其具有碱性,无法说明是弱电解质,C项错误;
D. OH﹣浓度相同的NH3H2O 和 NaOH 溶液分别加水稀释,由于弱电解质的电离随着稀释,电离程度会变大,所以离子浓度的变化幅度会比强电解质的小,由此可知I为NH3H2O , II为NaOH,D项正确;
答案选C。

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目