题目内容
设NA为阿伏伽德罗常数的值。下列说法正确的是( )
| A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B.50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| C.7.80 g Na2O2与5.85 g NaCl所含阴离子数相等 |
| D.常温常压下,18g H2O含有的氢原子数为3NA |

 C
C考查阿伏加德罗常数的有关计算和应用。氯气溶于水的反应是可逆反应,所以0.1molCl2溶于水,转移的电子数目小于0.1NA,A不正确;由于浓硫酸在和铜反应过程中,浓度会逐渐变稀,而稀硫酸与铜是不反应的,所以选项B不正确,生成SO2分子数目小于0.46NA;选项C正确,阴离子的物质的量都是0.1mol;18g水的物质的量是1mol,含有2mol氢原子,选项D不正确,答案选D。

练习册系列答案
相关题目

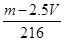 mol
mol 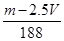 mol
mol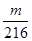 mol
mol