题目内容
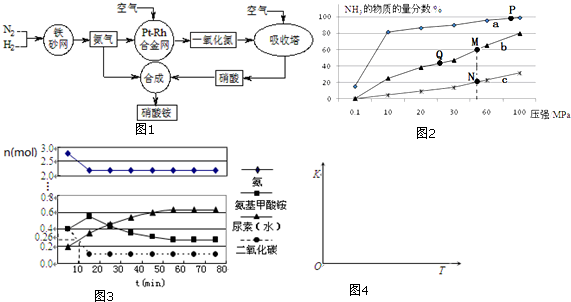
10. 2005年2月,我国政府就含有添加“苏丹红一号“色素的食品可能诱发癌症发出警告,并全面清剿苏丹红.“苏丹红一号“结构简式如图.有关“苏丹红一号“的下列叙述中不正确的是 ( )
2005年2月,我国政府就含有添加“苏丹红一号“色素的食品可能诱发癌症发出警告,并全面清剿苏丹红.“苏丹红一号“结构简式如图.有关“苏丹红一号“的下列叙述中不正确的是 ( )| A. | 分子式为C16H12N2O | |
| B. | 能与浓溴水发生取代反应 | |
| C. | 能与氯化铁溶液作用使溶液呈紫色 | |
| D. | 因苏丹红一号中含有酚羟基,故可被空气氧化产生醛基 |
分析 由结构可知分子式,分子中含N=N及酚-OH,结合不饱和键和酚的性质来解答.
解答 解:A.由结构可知分子式为C16H12N2O,故A正确;
B.含酚-OH,能与浓溴水发生取代反应,故B正确;
C.含酚-OH,能与氯化铁溶液作用使溶液呈紫色,故C正确;
D.含酚-OH,可被空气氧化,但不能产物-CHO,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团与性质的关系、酚的性质为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
20.某温度时,2NO(g)+O2(g)═2NO2(g)反应到2s后,NO的浓度减少了0.06mol•L-1,则以O2表示该时段的化学反应速率是( )
| A. | 0.03mol•L-1•s-1 | B. | 0.015mol•L-1•s-1 | ||
| C. | 0.12mol•L-1•s-1 | D. | 0.06mol•L-1•s-1 |
5.短周期元素A、B、C、D在周期表中的位置如右上图所示:B、D最外层电子数之和为12.
回答下列问题:
(1)与元素B、D处于同一主族的第2-5周期元素单质分别与H2反应生成1mol气态氢化物对应的热量变化如下,其中能表示该主族第4周期元素的单质生成1mol气态氢化物所对应的热量变化是b(选填字母编号).
a.吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8kJ
(2)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2.
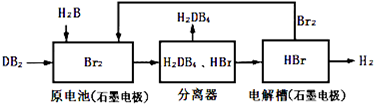
①查得:
试写出通常条件下电解槽中发生总反应的热化学方程式:2HBr(aq)=H2(g)+Br2(g)△H=+94kJ/mol
②根据资料:
为检验分离器的分离效果,取分离后的H2DB4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到无淡黄色沉淀出现,最终出现白色沉淀,证明分离效果较好.
③在原电池中,负极发生的反应式为SO2+2H2O-2e-=SO42-+4H+.
④在电解过程中,电解槽阴极附近溶液pH变大(填“变大”、“变小”或“不变”).
⑤将该工艺流程用总反应的化学方程式表示为:SO2+2H2O=H2+H2SO4.该生产工艺的优点有Br2被循环利用或能源循环供给或获得清洁能源(答一点即可).
(3)溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:海水提溴过程中,向浓缩的海水中通入Cl2,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO${\;}_{3}^{-}$,其离子方程式为3 Br2+6 CO32-+3H2O=5 Br-+BrO3-+6HCO3-(或3 Br2+3CO32-=5 Br-+BrO3-+3CO2↑).
回答下列问题:
| A | B | |
| C | D |
a.吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8kJ
(2)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2.

①查得:
| 化学键 | H-H | Br-Br | H-Br |
| 键能(kJ/mol) | 436 | 194 | 362 |
②根据资料:
| 化学式 | Ag2SO4 | AgBr |
| 溶解度(g) | 0.796 | 8.4×10-6 |
③在原电池中,负极发生的反应式为SO2+2H2O-2e-=SO42-+4H+.
④在电解过程中,电解槽阴极附近溶液pH变大(填“变大”、“变小”或“不变”).
⑤将该工艺流程用总反应的化学方程式表示为:SO2+2H2O=H2+H2SO4.该生产工艺的优点有Br2被循环利用或能源循环供给或获得清洁能源(答一点即可).
(3)溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:海水提溴过程中,向浓缩的海水中通入Cl2,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO${\;}_{3}^{-}$,其离子方程式为3 Br2+6 CO32-+3H2O=5 Br-+BrO3-+6HCO3-(或3 Br2+3CO32-=5 Br-+BrO3-+3CO2↑).
15.下列有关热化学方程式的书写及对应的表述均正确的是( )
| A. | 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成17.6 g硫化亚铁时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6 kJ•mol-1 | |
| B. | 稀醋酸与0.1 mol•L-1 NaOH溶液反应:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1 | |
| C. | 已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| D. | 已知2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则可知C的燃烧热△H=-110.5 kJ•mol-1 |
20.下列说法正确的是( )
| A. | 电离平衡常数受溶液浓度的影响 | |
| B. | 电离平衡常数不可以表示弱电解质的相对强弱 | |
| C. | 电离常数越大的酸,其溶液的 c(H+)一定越大 | |
| D. | H2CO3的第一步电离的电离常数表达式:K=$\frac{c({H}^{+})•c(HC{O}_{3}^{-})}{c({H}_{2}C{O}_{3})}$ |