题目内容
在密闭容器中发生下列反应aA(g)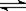 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
| A.A的转化率增大 | B.平衡向正反应方向移动 |
| C.D的体积分数变大 | D.a < c+d |
D
解析试题分析:气体体积刚压缩平衡还未移动时D的浓度是原来的2倍,当再次达到平衡时,D的浓度为原平衡的1.8倍,D的浓度减小,所以压缩体积使平衡向逆反应方向移动。A选项,平衡向逆反应方向移动,A的转化率变小,故A错误;B选项,平衡向逆反应方向移动,故B错误;C选项,平衡向逆反应方向移动,D的体积分数减小,故C错误;D选项,增大压强,平衡向气体体积减小的方向移动,该平衡向逆反应方向移动,所以a<c+d,故D正确。
考点:化学平衡的影响因素;化学平衡的计算

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在密闭容器中发生下列反应aA(g) cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.6倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.6倍,下列叙述正确的是
| A.A的转化率变大 | B.平衡向正反应方向移动 |
| C.D的质量分数变大 | D.a<c+d |
硫代硫酸钠与稀盐酸的反应Na2S2O3+2HCl→2NaCl+S↓+SO2↑+H2O在加热条件下反应速度加快,原因主要是
| A.该反应是吸热反应,且可逆,加热使平衡向正向移动 |
| B.加热促使SO2逸出,使平衡向正向移动 |
| C.加热促进S2O32-与H+的碰撞,使反应加速 |
| D.加热促进Na+与Cl-的碰撞,使反应加速 |
已知A(s)+2B(g)  2C(g)+D(g) △H<0 在一密闭容器中反应的υ-t图。t1时,改变了一个条件,下列叙述正确的是
2C(g)+D(g) △H<0 在一密闭容器中反应的υ-t图。t1时,改变了一个条件,下列叙述正确的是
| A.t1时,一定是升高了反应的温度 |
| B.t1时,可能是向容器中通入了一定量的C气体 |
| C.t1时,可能是向容器中加入了催化剂 |
| D.t1时改变外界条件后,该反应的平衡常数可能减小,也可能不变 |
化学反应C(s)+H2O(g) CO(g)+H2(g);△H>0达到平衡,下列叙述正确的是
CO(g)+H2(g);△H>0达到平衡,下列叙述正确的是
| A.升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
| B.加入固体碳,平衡向正反应方向移动 |
| C.加入水蒸气使容器压强增大,平衡向逆反应方向移动动 |
| D.减小压强,平衡向正反应方向移 |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y
 2Z,其平衡常数值为1600
2Z,其平衡常数值为1600C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
 2CO; △H1>0,反应速率ν1 N2+3H2
2CO; △H1>0,反应速率ν1 N2+3H2 和
和 的变化是
的变化是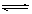 A2(g) +3B2(g)(正反应吸热)下列图像正确的是
A2(g) +3B2(g)(正反应吸热)下列图像正确的是