题目内容
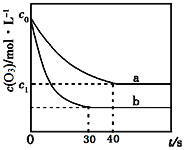
【题目】臭氧的脱硝反应为:2NO2(g) + O3(g)![]() N2O5(g) + O2(g),一定条件下,向2.0L恒容密闭容器中充入2.0molNO2和1.0 molO3,一段时间后达到平衡。下图曲线a表示该反应在温度T下O3的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时O3的浓度随时间的变化。下列叙述正确的是( )
N2O5(g) + O2(g),一定条件下,向2.0L恒容密闭容器中充入2.0molNO2和1.0 molO3,一段时间后达到平衡。下图曲线a表示该反应在温度T下O3的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时O3的浓度随时间的变化。下列叙述正确的是( )
A. 反应2NO2(g) + O3(g)![]() N2O5(g) + O2(g) △S<0
N2O5(g) + O2(g) △S<0
B. 曲线b对应的条件改变可能是加入了催化剂,平衡常数Ka=Kb
C. 曲线b对应的条件改变可能是密闭容器的体积变为4.0L
D. 若c1=0.3mol·L-1,从反应开始到平衡时该反应的速率v(NO2)=0.005 mol·L-1·s-1
【答案】A
【解析】
试题A、正反应气体物质的量减小,混乱度减小,则△S<0,故A正确;B、加入催化剂加快反应速率,不影响平衡移动,O3的浓度不变,但图象中O3的浓度减小,可能是增大二氧化氮浓度,也可能是改变温度,平衡常数不一定相等,故B错误;C、若体积变为4.0 L,压强减小,平衡逆向移动,平衡时O3浓度大于a中O3浓度的![]() ,图象中平衡时b条件下O3浓度等于a中O3浓度的
,图象中平衡时b条件下O3浓度等于a中O3浓度的![]() ,故C错误;D、v(O3)=
,故C错误;D、v(O3)=![]() ="0.005" molL-1s-1,速率之比等于化学计量数之比,v(NO2)=2v(O3)="0.01" molL-1s-1,故D错误,故选A。
="0.005" molL-1s-1,速率之比等于化学计量数之比,v(NO2)=2v(O3)="0.01" molL-1s-1,故D错误,故选A。

练习册系列答案
相关题目