题目内容
氢燃料电池公交汽车已经驶上了一些城市的街头.下列说法正确的是( )
| A、电解水制取氢气是理想且经济的制氢方法 |
| B、利用化石燃料燃烧放热使水分解是理想的制氢方法 |
| C、氢燃料电池汽车的使用可以有效减少城市空气污染 |
| D、发展氢燃料电池汽车不需要安全、高效的储氢技术 |
考点:原电池和电解池的工作原理,清洁能源
专题:电化学专题
分析:A、电解水制取氢气消耗大量的电能;
B、化石燃料燃烧放热使水分解会消耗大量能源;
C、氢氧燃料电池的产物是水;
D、氢气密度小,安全高效的储氢技术是难题.
B、化石燃料燃烧放热使水分解会消耗大量能源;
C、氢氧燃料电池的产物是水;
D、氢气密度小,安全高效的储氢技术是难题.
解答:
解:A、电解水制取氢气消耗大量的电能,电解水制取氢气是理想而经济的制氢方法,故A错误;
B、水不容易分解,而且利用化石燃料燃烧放热使水分解会消耗大量能源,故B错误;
C、氢氧燃料电池的生成产物是水,环保无污染,所以氢燃料电池汽车的使用可以有效减少城市空气污染,故C正确;
D、氢气密度小,发展氢燃料电池汽车,安全高效的储氢技术是难题,故D正确.
故选C.
B、水不容易分解,而且利用化石燃料燃烧放热使水分解会消耗大量能源,故B错误;
C、氢氧燃料电池的生成产物是水,环保无污染,所以氢燃料电池汽车的使用可以有效减少城市空气污染,故C正确;
D、氢气密度小,发展氢燃料电池汽车,安全高效的储氢技术是难题,故D正确.
故选C.
点评:本题考查燃料电池的能量转化以及工作原理,是化学和实际结合的知识考查,题目难度不大.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、1L 0.1mol?L-1的氨水中含有的NH3?H2O分子数为0.1NA |
| B、电解精炼铜时,若阳极质量减少6.4g,则电路中转移电子数为0.2NA |
| C、标准状况下,2.24L的二氯甲烷中含有的碳氯共价键的数目为0.2NA |
| D、一定条件下,4.6g NO2和N2O4混合气体中含有的N原子数目为0.1NA |
下列实验能达到预期目的是( )
①用硝酸钡溶液鉴别硫酸根离子与亚硫酸根离子;
②用溴水检验汽油中是否含有不饱和链烃;
③用乙醇从碘水中萃取碘;
④用盐析方法分离提纯蛋白质;
⑤用加热方法提纯含有少量碳酸氢钠的碳酸钠固体;
⑥闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔.
①用硝酸钡溶液鉴别硫酸根离子与亚硫酸根离子;
②用溴水检验汽油中是否含有不饱和链烃;
③用乙醇从碘水中萃取碘;
④用盐析方法分离提纯蛋白质;
⑤用加热方法提纯含有少量碳酸氢钠的碳酸钠固体;
⑥闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔.
| A、②④⑤⑥ | B、①③⑥ |
| C、①②④⑤⑥ | D、②③④⑤ |
如图为氢氧燃料电池的原理示意图,按照此图的提示,下列叙述中不正确的是( )
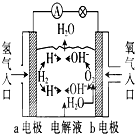

| A、a电极是负极 |
| B、b电极的电极反应式为4OH--4e-═2H2O+O2↑ |
| C、在电池内部,H+向b电极附近运动 |
| D、氢氧燃料电池是一种具有广泛应用前景的绿色电源 |
下列物质既含有共价键又含有离子键的是( )
| A、H2SO4 |
| B、CO2 |
| C、Na2O2 |
| D、CaCl2 |
下列各醇中,既能发生消去反应又能发生催化氧化反应的是( )
| A、CH3-OH |
B、 |
C、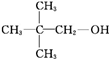 |
D、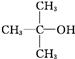 |
在通常条件下,下列各组物质的性质排列正确的是( )
| A、水溶性:NH3>H2S>I2 |
| B、沸点:HF>HCl>HBr |
| C、硬度:金刚石>晶体硅>碳化硅 |
| D、熔点:LiF>KF>NaF |
下列关于丙烯(CH3-CH=CH2)的说法正确的是( )
| A、丙烯分子有7个δ键,1个π键 |
| B、丙烯分子中3个碳原子都是sp3杂化 |
| C、丙烯分子中所有原子在同一平面上 |
| D、丙烯分子存在非极性键 |
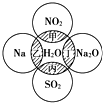 图中两圆圈相交的阴影部分表示圆圈内物质相互发生的反应,其中属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )
图中两圆圈相交的阴影部分表示圆圈内物质相互发生的反应,其中属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )