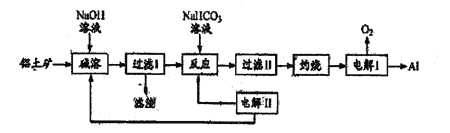
��Ŀ����
����Ŀ����1��ȡ����Fe2O3��ĩ(����ɫ)�����������ᣬ������Ӧ�Ļ�ѧ����ʽ��____________________����Ӧ��õ�����Һ��________ɫ���ô���Һ�ֱ�������ʵ�飺
��2����С�ձ��м���20 mL����ˮ�����������ں����ˮ�е��뼸�α���FeCl3��Һ�������������Һ��________ɫ��ֹͣ���ȣ����Ƶ�Fe(OH)3���塣
��3�����ƵõĽ�������Ĥ�ƳɵĴ��ڣ���ͼ��ʾ������2 min��ȡ������Ĥ���Һ�����Թ��У����ڰ�������һ��ǿ��Ӳ������䣬�۲�________(��С����ޡ�)������������ʵ�������������___________________�������Թ��м�����ϡ�����ữ����������Һ���ɹ۲쵽������Ϊ___________________________________________
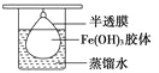
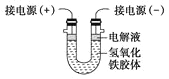
��4������Ĥ�ڵ�Һ�嵹��U�ι��У���ͼ��ʾ����Һ���Ϸ������������Һ�Ա������壬��ֱͨ����۲쵽��������________(����������������)��������ɫ�����ԭ����__________________________________��
���𰸡�Fe2O3��6HCl===2FeCl3��3H2O�ػƺ���������Һ�а�ɫ����������Fe(OH)3���������磬ͨ����������ƶ�
��������
��1�����ݽ������������ᷴӦ�����κ�ˮ��д����Ӧ�Ļ�ѧ����ʽ��
��2��Fe(OH)3����ʺ��ɫ��
��3�����������ЧӦ��������Һ�ͽ��壬����������Ĥ���������ܣ�
��4��Fe(OH)3���������磬ͨ����������ƶ���
��1��Fe2O3��ĩ������ɫ�������������ᣬ�������ķ�Ӧ�Ļ�ѧ����ʽΪ��Fe2O3 +6HCl=2FeCl3 +3H2O����Ӧ��õ�����Һ���ػ�ɫ��
��2��Fe(OH)3����ʺ��ɫ��
��3������������Ĥ���������ܣ�ȡ������Ĥ���Һ�����Թ��У����ڰ�������һ��ǿ��Ӳ������䣬�۲�������������ʵ������������������Һ�������Թ��м�����ϡ�����ữ����������Һ�����������ӣ��ɹ۲쵽������Ϊ�а�ɫ�������ɣ�
��4��Fe(OH)3���������磬�ڵ糡�����·�����Ӿ��������ɵĽ����������ƶ���������������ɫ���