题目内容
下列物质中,在标准状况下体积最大的是( )
| A.900g H2O | B.71g Cl2 | C.48g O2 | D.28g N2 |
C
解析试题分析:A、水在标准状况下为液体,900gH2O的体积为0.9L;B、Cl2的物质的量为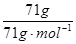 =1mol,22.4L;C、O2的物质的量为
=1mol,22.4L;C、O2的物质的量为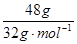 =1.5mol,D、N2的物质的量为
=1.5mol,D、N2的物质的量为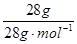 =1mol;显然C的物质的量最大,其体积最大为1.5mol×22.4L·mol-1=33.6L,选C.
=1mol;显然C的物质的量最大,其体积最大为1.5mol×22.4L·mol-1=33.6L,选C.
考点:物质的量的相关计算;气体摩尔体积

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
设NA代表阿伏加德罗常数,下列叙述正确的是 ( )
| A.标准状况下2.24 L H2O中,分子数为0.1NA |
| B.将1mol Cl2通入到水中,则N(HClO)+ N(Cl?)+ N(ClO-)= 2NA |
| C.常温常压下16g O2和O3混合气体中,氧原子数为NA |
| D.7.8g Na2O2与足量水反应,转移电子数为0.2NA |
设NA为阿伏加德罗常数的数值,下列叙述中正确的是
| A.常温常压下,100g8.5%的H2O2水溶液中含氧原子总数为NA |
| B.标准状况下,NA个H2O分子所占的休积为22.4L |
| C.标准状况下,2.24L乙烯分子中σ键为0.1NA |
| D.常温常压下,4.8g臭氧与4.8g氧气所含的氧原子数均为0.3NA |
将23g Na和24g Mg分别投入等质量的过量的盐酸中,反应完毕后,所得溶液的质量分数分别为m和n,则m和n的关系是
| A.m>n | B.m=n | C.m<n | D.无法确定 |
下列化学用语书写正确的是
| A.氢气分子的电子式:H∶H |
B.硫原子的结构示意图: |
C.溴化钠的电子式: |
D.苯的分子式: |
某氯原子的质量为a g , C-12原子的质量为b g,用NA表示阿伏加德罗常数,下列说法中不正确的是
A.则该氯原子构成氯分子的相对分子质量为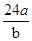 |
| B.1mol该氯原子的质量为aNAg |
C.mg该氯原子的物质的量为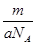 mol mol |
D.ng该氯原子所含的电子数为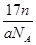 |
今有一包铁粉和铜粉混合粉末,为确定其组成,现提供4 mol·L-1的FeCl3溶液(其它用品略),某合作学习小组同学的实验结果如下(假定反应前后溶液体积不变):
| 组别 | ① | ② | ③ | ④ |
| V[FeCl3(aq)]/mL | 100 | 100 | 100 | 100 |
| 混合粉末质量/g | 6 | 13.2 | 24 | 36 |
| 反应后剩余固体质量/g | 0 | 1.28 | 12.8 | 24.8 |
下列结论正确的是( )
A.第①组反应后溶液中c(Fe3+) =" 3.0" mol·L-1
B.第②组剩余固体是铜铁混合物
C.第④组反应后的滤液中c(Fe2+) =" 6" mol·L-1
D.原混合粉末中n(Fe)∶n(Cu) = 3∶2
以色列科学家Daniel Shechtman因发现准晶体获得2011年诺贝尔化学奖。人们在自然界中也找到了组成为Al63Cu24Fe13的天然准晶体。将相同质量的此准晶体分别与足量的盐酸、烧碱和稀硝酸反应,产生气体的物质的量关系为
| A.n(烧碱)<n(稀硝酸)<n(盐酸) |
| B.n(烧碱)<n(盐酸)<n(稀硝酸) |
| C.n(稀硝酸)<n(烧碱)<n(盐酸) |
| D.n(盐酸)<n(稀硝酸)<n(烧碱) |
下列数量的物质中含原子数最多的是
| A.4℃时5.4mL水 | B.标准状况下5.6L二氧化碳 |
| C.0.4mol氧气 | D.10g氖 |