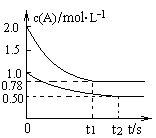题目内容
一定条件下存在反应:CO(g)+H2O(g) CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
| A.容器Ⅰ、Ⅱ中正反应速率相同 |
| B.容器Ⅰ中CO的转化率与容器Ⅱ中CO2的转化率之和小于1 |
| C.容器Ⅰ中CO的物质的量比容器Ⅱ中的少 |
| D.容器Ⅰ、Ⅲ中反应的平衡常数相同 |
B
解析试题分析:A.容器Ⅰ、Ⅱ中是从正反应、逆反应两个相反的方向开始进行的。该反应的正反应为放热反应,反应在恒容绝热密闭容器所以反应进行,所以达到平衡时的正反应速率不会相同。错误。B.若反应是在相同的温度下进行,则容器Ⅰ中CO的转化率与容器Ⅱ中CO2的转化率之和等于1。但是由于反应是在恒容绝热密闭容器所以反应进行,二者转化率的和必小于1.正确。C.容器Ⅰ中反应从正反应方向开始,随着反应的进行,温度升高。升高温度,化学平衡逆向移动;而容器Ⅱ中是从逆反应方向开始,随着反应的进行,容器的温度会降低。降低温度,化学平衡向放热反应方向移动,CO的物质的量会增大。所以都达到平衡时容器Ⅰ中CO的物质的量比容器Ⅱ中的大。错误。D.容器Ⅲ中各物质的物质的量浓度增大,增大浓度化学平衡正向移动,容器的温度升高。升高温度,化学平衡向吸热反应方向移动。所以容器Ⅰ、Ⅲ中反应的平衡常数不相同。错误。
考点:考查在浓度、温度对可逆反应的各物质的化学平衡常数、浓度转化率的影响的知识。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案可逆反应H2(g)+I2(g)  2HI(g)在密闭容器中反应,达到平衡状态时的标志是( )
2HI(g)在密闭容器中反应,达到平衡状态时的标志是( )
| A.混合气体的密度不再改变 | B.混合气体的颜色不再改变 |
| C.混合气体的压强不再改变 | D.I2、H2在混合气体中的体积分数相等 |
COCl2(g) CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |
下列事实能用勒沙特列原理解释的是( )
①由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
②实验室中用氯化钠固体与浓硫酸共热制取氯化氢气体
③用排饱和食盐水法收集Cl2
④温度控制在500℃有利于合成氨反应
⑤工业制
取金属钾Na(l)+ KCl(l)  NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
| A.②③⑤ | B.①③⑤ | C.①②③④⑤ | D.①②③⑤ |
在容积为1L的密闭容器中,充入1mol CO2和3mol H2,在温度500℃时发生反应:CO2(g)+ 3H2(g) CH3OH(g)+ H2O(g)△H<0。CH3OH的浓度随时间变化如图,下列说法不正确的是
CH3OH(g)+ H2O(g)△H<0。CH3OH的浓度随时间变化如图,下列说法不正确的是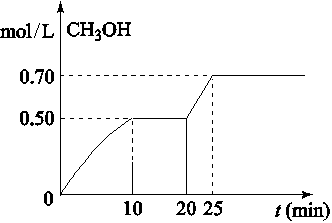
| A.从反应开始到10分钟时,H2的平均反应速率v(H2)=0.15 mol/(L·min) |
| B.从20分钟到25分钟达到新的平衡,可能是增大压强 |
| C.其它条件不变,将温度升到800℃,再次达平衡时平衡常数减小 |
| D.从开始到25分钟,CO2的转化率是70% |
α1和α2分别为A在甲、乙两个恒容容器中平衡体系A(g) 2B(g)和2A(g)
2B(g)和2A(g) C(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是( )
C(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是( )
| A.α1、α2均减小 | B.α1、α2均增大 |
| C.α1减小,α2增大 | D.α1增大,α2减小 |
使2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g) 2NH3(g)(正反应为放热反应)。下列说法错误的是
2NH3(g)(正反应为放热反应)。下列说法错误的是
| A.升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量变大 |
| B.升高平衡体系的温度(保持体积不变),混合气体的密度不变 |
| C.当反应达到平衡时,N2和H2的浓度比是1∶3 |
| D.当达到平衡时,充入氩气,并保持压强不变,平衡将逆向移动 |
下列叙述不正确的是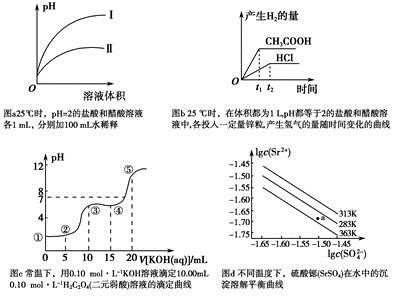
| A.图a中,曲线Ⅱ表示醋酸溶液加100 mL水稀释的图像 |
| B.图b中,可能各投入的锌粒颗粒大小相同且质量均为0.65 g |
| C.图c中,在①、②、③、④、⑤各点的溶液中所含阴离子种类不同 |
| D.图d中,三个不同温度中,313 K时Ksp(SrSO4)最大;且283 K时,图中a点对应的溶液是不饱和溶液 |
 xC(g) △H<0,测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是
xC(g) △H<0,测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是