题目内容
11.下列化合物中所有化学键都是共价键的是( )| A. | Na2O2 | B. | NaOH | C. | BaCl2 | D. | H2SO4 |
分析 一般来说,活泼金属元素与活泼非金属元素形成离子键,非金属之间形成共价键,以此来解答.
解答 解:A.Na2O2中既有离子键又有共价键,故A不选;
B.NaOH中既有离子键有有共价键,故B不选;
C.BaCl2中,只有离子键,故C不选;
D.H2SO4中,存在H-O、S-O、S=O等共价键,故D选;
故选D.
点评 本题考查化学键,注意把握化学键判断的一般规律即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
1.下列说法正确的是( )
| A. | 溶液是呈电中性的,而胶体是可以带电的 | |
| B. | 向沸水中加入FeCl3饱和溶液,继续煮沸至溶液呈红褐色时即得到Fe(OH)3胶体 | |
| C. | 清晨,阳光透过树叶间的缝隙可以产生丁达尔效应,说明空气是一种胶体 | |
| D. | 常用于区分溶液和胶体的方法是利用丁达尔效应,属于化学方法 |
19.下列说法不正确的是( )
| A. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
| B. | 吸热反应在一定条件(如常温、加热等)也能发生 | |
| C. | 放热反应都不需要加热就能发生 | |
| D. | 化学反应是放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量 |
6.下列与处理方法对应的反应方程式不正确的是( )
| A. | 工业上用水吸收NO2生产硝酸:3NO2+H2O═2HNO3+NO | |
| B. | 用氨水除去工业原料氯化铵中的氯化铁杂质:Fe3++3OH-═Fe(OH)3↓ | |
| C. | 用熟石灰处理泄漏的液氯:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O | |
| D. | 用明矾除去水中的悬浮颗粒物:Al3++3H2O?Al(OH)3 (胶体)+3H+ |
16.足量铜溶于一定量浓硝酸,产生NO2、N2O4、NO的混合气体,这些气体若与2.24LO2(标准状况)混合后通入水中,气体被水完全吸收.若向原所得溶液中加入l0mol•L-1H2SO4溶液100mL,则继续溶解的Cu的质量为( )
| A. | 0 | B. | 32g | C. | 38.4g | D. | 48g |
20. 恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
 恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )| A. | t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 | |
| B. | Z和W在该条件下都不为气态 | |
| C. | 若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等 | |
| D. | 若该反应只在某温度T0以上才能进行,则该反应的平衡常数K随温度升高而减小 |
1.下列实验方法能达到实验目的是( )
| A. | 用铂丝蘸取某未知溶液于酒精灯火焰上灼烧,显黄色,证明该溶液不含K+ | |
| B. | 萃取碘水中的碘时,可以选择苯或四氯化碳作为萃取剂 | |
| C. | 某溶液中先加氯水,再滴加KSCN溶液出现血红色,证明溶液中含有Fe2+ | |
| D. | 某无色溶液中加硝酸银溶液产生白色沉淀,再加稀盐酸沉淀不消失,证明原溶液中含有Cl- |
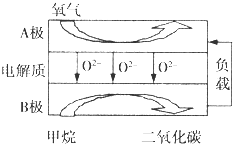 甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.
甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.