题目内容
19.实验室有A、B、C、D四个装置,请回答下列各题: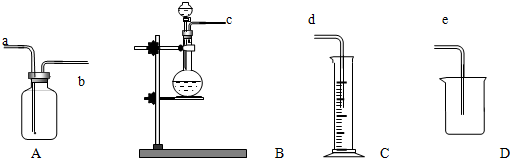
(1)若A作为集气装置,收集下列气体:H2、Cl2、NH3、NO、NO2、CO2
①若收集NH3(A装置不能移动,改装),则气体由b进口(填a、b字母);
②若将A装置进行排水法集气,则气体由b进口(填a、b字母),可以收集上述气体中的H2、NO气体;
(2)实验室检查B装置气密性的操作方法是将c连接的导管放入盛放水的水槽中,加热烧瓶,观察到水槽中有气泡冒出,则气密性良好.
(3)实验室可选用A、B、C、D中的仪器和装置,组装一套测定某活泼金属(以Na为例)的相对原子质量的实验装置,各导管接口的连接顺序为c→b→a→d(填字母).
分析 (1)①氨气的密度比空气的密度小,应利用向下排空气收集;
②若将A装置进行排水法集气,应将水排出,导管短进;可收集不溶于水的气体;
(2)利用微溶法检验气密性;
(3)测定某活泼金属(以Na为例)的相对原子质量的实验装置,利用B装置发生钠与水的反应,A、C装置排水测定氢气的体积,即可计算测定.
解答 解:(1)①氨气的密度比空气的密度小,应利用向下排空气收集,则气体从b进口进入,故答案为:b;
②若将A装置进行排水法集气,应将水排出,导管短进,则气体从b进入;可收集不溶于水的气体,有H2、NO,故答案为:b;H2、NO;
(2)实验室检查B装置气密性的操作方法是将c连接的导管放入盛放水的水槽中,加热烧瓶,观察到水槽中有气泡冒出,则气密性良好,
故答案为:将c连接的导管放入盛放水的水槽中,加热烧瓶,观察到水槽中有气泡冒出,则气密性良好;
(3)测定某活泼金属(以Na为例)的相对原子质量的实验装置,利用B装置发生钠与水的反应,A、C装置排水测定氢气的体积,即可计算测定,则各导管接口的连接顺序为c→b→a→d,故答案为:c→b→a→d.
点评 本题考查实验装置综合,为高频考点,把握物质的性质、气密性检验、气体的收集、实验装置的作用为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
9. 目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2+3H2?CH3OH+H2O,该反应的能量变化如图所示:
目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2+3H2?CH3OH+H2O,该反应的能量变化如图所示:
(1)甲同学认为该反应为放热反应,他的理由为:反应物的总能大于生成物的总能量
(2)在体积为2L的密闭容器中,充入1mol CO2和3mol H2,测得CO2的物质的量随时间变化如表所示.从反应开始到5min末,用CO2浓度变化表示的平均反应速率v(CO2)=0.05mol/(L.min);
反应达到平衡状态,此时H2的转化率为75%.
(3)在相同温度、容积不变的条件下,能说明该反应已达平衡状态的是bd(填序号).
a.v生成(CH3OH)=v消耗(CO2)
b.CO2、H2、CH3OH、H2O的浓度均不再变化
c.n(CO2):n(H2):n(CH3OH):n(H2O)=1:1:1:1
d.H2的消耗速率与CH3OH的消耗速率之比为3:1.
 目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2+3H2?CH3OH+H2O,该反应的能量变化如图所示:
目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2+3H2?CH3OH+H2O,该反应的能量变化如图所示:(1)甲同学认为该反应为放热反应,他的理由为:反应物的总能大于生成物的总能量
(2)在体积为2L的密闭容器中,充入1mol CO2和3mol H2,测得CO2的物质的量随时间变化如表所示.从反应开始到5min末,用CO2浓度变化表示的平均反应速率v(CO2)=0.05mol/(L.min);
反应达到平衡状态,此时H2的转化率为75%.
| t/min | 0 | 2 | 5 | 10 | 15 |
| n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
a.v生成(CH3OH)=v消耗(CO2)
b.CO2、H2、CH3OH、H2O的浓度均不再变化
c.n(CO2):n(H2):n(CH3OH):n(H2O)=1:1:1:1
d.H2的消耗速率与CH3OH的消耗速率之比为3:1.
14.在1L密闭容器中通入2mol 氨气,在一定温度下发生反应:2NH3?N2+3H2,达平衡时,N2的物质的量分数为a%,维持容器的体积和温度不变,分别通入下列几组物质,达到平衡时,容器内N2的物质的量分数仍为a%的是( )
| A. | 3 mol H2和1 mol N2 | |
| B. | 2 mol NH3和1 mol N2 | |
| C. | 2 mol N2和3 mol H2 | |
| D. | 0.1 mol NH3、0.9 mol N2、2.85 mol H2 |
11.原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为2n2-1.下列有关X的说法中不正确的是( )
| A. | X能与某些非金属元素化合 | |
| B. | X可能为金属元素 | |
| C. | X原子的最外层电子数和核电荷数肯定为奇数 | |
| D. | X可能形成化学式为KXO3的盐 |
8.下列各反应的化学方程式中,不正确的是( )
| A. | 将点燃的镁条伸入充满CO2气体的集气瓶中:2Mg+CO2═点燃 2MgO+C | |
| B. | 大理石溶于醋酸:CO32-+2CH3COOH═2CH3COO-+CO2↑+H2O | |
| C. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-═BaSO4↓+NH3•H2O+H2O | |
| D. | 向淀粉KI溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝:4H++4I-+O2═2I2+2H2O |
9.下列式子表示的物质一定为纯净物的是( )
| A. | C2H6 | B. | C4H10 | C. | C5H12 | D. | C7H16 |

 .
.