题目内容
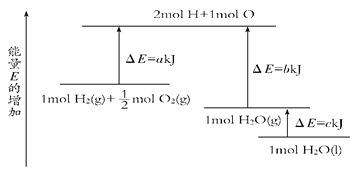
【题目】一定条件下,化学反应2H2+O2===2H2O的能量变化如图所示,则反应的热化学方程式可表示为( )
A. H2(g)+1/2O2(g)===H2O(g)ΔH=(a+b) kJ·mol-1
B. 2H2(g)+O2(g)===2H2O(g)ΔH=2(b-a) kJ·mol-1
C. H2(g)+1/2O2(g)===H2O(l)ΔH=(b+c-a) kJ·mol-1
D. 2H2(g)+O2(g)===2H2O(l)ΔH=2(a-b-c) kJ·mol-1
【答案】D
【解析】试题分析:反应热等于反应物总能量减去生成物总能量,根据图像可知H2(g)+1/2O2(g)===H2O(g) ΔH=(a-b) kJ/mol,H2(g)+1/2O2(g)===H2O(l) ΔH=(a-b-c) kJ/mol,所以有2H2(g)+O2(g)===2H2O(g) ΔH=2(a-b) kJ/mol或 2H2(g)+O2(g)===2H2O(l) ΔH=2(a-b-c) kJ/mol,答案选D。

【题目】相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应,下列说法正确的是
A. 强酸溶液产生较多的氢气 B. 弱酸溶液产生较多的氢气
C. 两者产生等量的氢气 D. 无法比较两者产生氢气的量
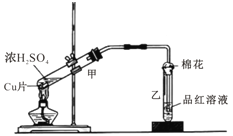
【题目】右图为浓硫酸与铜片反应的装置。
请回答:
(1)浓硫酸与铜片反应的化学方程式为 。
(2)反应一段时间后,试管乙中品红溶液的现象是 。
(3)下列有关该实验的说法中,不正确的是 。
A.该反应中浓硫酸只体现酸性 |
B.试管乙中含有碱液的棉花,其作用是吸收过量的SO2,防止环境污染 |
C.反应一段时间后,将试管甲中的溶液缓慢倒入盛有水的烧杯,溶液显蓝色 |
D.含0.04mol溶质的浓硫酸与足量的铜片反应,能收集到448mL的SO2(标准状况) |