题目内容
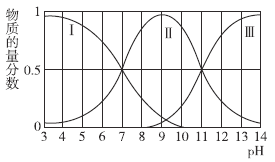
【题目】常温下,向二元弱酸H2A溶液中滴加NaOH溶液,不同pH时,相关微粒的物质的量分数如图所示,下列说法正确的是( )
A.pH=7时,溶液中c(Na+)=c(H2A)
B.pH=9时,c(OH-)=c(H2A)+c(H+)
C.pH=3和pH=11时,溶液中水的电离程度完全相同
D.H2A的一级电离常数和二级电离常数相差2个数量级
【答案】A
【解析】
A.由图分析知I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,根据电荷守恒:2c(A2-)+c(HA- )+c(OH-)=c(Na+)+c(H+),pH=7时,c(A2-)=0,c(HA-)=c(H2A)可知c(Na+)=(H2A),故A正确;
B.pH=9时,为NaHA溶液,根据物料守恒和电荷守恒可知c(A2-)+c(OH-)=c(H2A)+c(H+),故B错误;
C.pH=3时溶液中的溶质主要为H2A,水的电离被抑制,pH=11时溶液中的溶质为NaHA和Na2A,溶液显碱性,促进水的电离,故C错误;
D.H2A的一级电离常数为10-7,H2A的二级电离常数为10-11,H2A的一级电离常数和二级电离常数相差4个数量级,故D错误;
故选A。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
【题目】读下列药品标签,有关分析不正确的是( )
选项 | A | B | C | D |
物品标签 | 饱和氯水1.01×105 Pa,20 ℃ | 药品:×××
| 碳酸氢钠NaHCO3俗名小苏打(84 g·mol-1) | 浓硫酸H2SO4 密度1.84 g·mL-1浓度98.0% |
分析 | 该试剂应装在橡胶塞的细口瓶中 | 该药品不能与皮肤直接接触 | 该物质受热易分解 | 该药品标签上还标有
|
A. AB. BC. CD. D