��Ŀ����
����Ŀ�����������ھ�������������ˮ��������������ҵ���������������
��1���������������������ҿ������������е��ʷ�Ӧ���磺6Ag��s��+O3��g���T3Ag2O��s����H=��235.8kJ/mol��
��֪2Ag2O��s���T4Ag��s��+O2��g����H=+62.2kJ/mol��
�����·�Ӧ��2O3��g���T3O2��g���ġ�H= ��
��2����ѧ������ʹ�������������µ��ˮ�ķ����Ƶó�����������������Χ��ˮ�в������缫��ӦʽΪ3H2O��6e��=O3��+6H+ �� ���������ܽ���ˮ�е��������ɹ������⣬��缫��ӦʽΪ ��
��3��O3�ڼ��������¿ɽ�Na2SO4������Na2S2O8������������д���÷�Ӧ�Ļ�ѧ����ʽ��
��4�����õ�Na2S2O8��Һ�ɽ����л���Ⱦ��4��CP��ԭ����Na2S2O8��Һ��һ�������¿ɲ���ǿ���������ɻ���SO4������ͨ���ⶨ4��CP�����ʿ��ж�Na2S2O8��Һ����SO4��������ij�о�С�����ʵ��̽������Һ����ԡ�Fe2+��Ũ�ȶԲ���SO4����Ӱ�죮����Һ����Ե�Ӱ�죺����������ͬ����4��CP���뵽��ͬpH��Na2S2O8��Һ�У������ͼa��ʾ���ɴ˿�֪����Һ������ǿ����������ڡ������ڡ���Na2S2O8����SO4�� �� 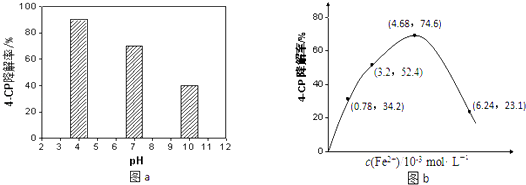
��Fe2+Ũ�ȵ�Ӱ�죺��ͬ�����£�����ͬŨ�ȵ�FeSO4��Һ�ֱ����c��4��CP��=1.56��10��4molL��1��c��Na2S2O8��=3.12��10��3 molL��1�Ļ����Һ�У���Ӧ240min����ʵ������ͼb��ʾ����֪ S2O82��+Fe2+�TSO4��+SO42��+Fe3+ �� ����ͼʾ��֪����˵����ȷ���ǣ�������ţ�
A����Ӧ��ʼһ��ʱ����4��CP��������Fe2+Ũ�ȵ����������ԭ����Fe2+��ʹNa2S2O8���������SO4����
B��Fe2+��4��CP���ⷴӦ�Ĵ���
C����c��Fe2+������ʱ��4��CP�����ʷ����½���ԭ�������Fe2+����SO4��������Ӧ�����IJ���SO4����
D��4��CP�����ʷ����½���ԭ����������ɵ�Fe3+ˮ��ʹ��Һ��������ǿ��������4��CP�Ľ��⣮
�۵�c��Fe2+��=3.2��10��3molL��1ʱ��4��CP�����ƽ����Ӧ���ʵļ������ʽΪ ��
���𰸡�
��1����285.0kJ?mol��1
��2��3O2+6H++6e��=3H2O2����O2+2H++2e��=H2O2��
��3��2Na2SO4+O3+H2O=Na2S2O8+2NaOH+O2
��4�������ڣ�AC��![]()
���������⣺��1����6Ag��s��+O3��g���T3Ag2O��s������H=��235.8kJmol��1 �� ��2Ag2O��s���T4Ag��s��+O2��g������H=+62.2kJmol��1 ��
���ݸ�˹���ɿ�֪�١�2+�ڡ�3�ɵõ���2O3��g���T3O2��g������Ӧ�ȡ�H=����235.8kJmol��1����2+��+62.2kJmol��1����3=��285kJ/mol��
���Դ��ǣ���285kJ/mol����2�����������µ��ˮ�ķ����Ƶó�����������������Χ��ˮ�в�������缫��ӦʽΪ3H2O��6e���TO3��+6H+ �� ���������������õ������ɹ������⣬��缫��ӦʽΪ3O2+6H++6e���T3H2O2 ��
���Դ��ǣ�3O2+6H++6e���T3H2O2����O2+2H++2e��=H2O2������3��O3�ڼ��������¿ɽ�Na2SO4������Na2S2O8�����������ķ���ʽΪ��2Na2SO4+O3+H2O=Na2S2O8+2NaOH+O2 �� ���Դ��ǣ�2Na2SO4+O3+H2O=Na2S2O8+2NaOH+O2����4���ٸ�����Һ��pH��4��CP�Ľ����ʿ���֪����Һ������ǿ��������Na2S2O8����SO4�� �� ���Դ��ǣ������ڣ�
��A��������Һ��pH��4��CP�Ľ����ʿ���֪����Һ������ǿ��������Na2S2O8����SO4�� �� ��A��ȷ��
B�����Ի�����4��CP���ⷴӦ�Ĵ�������B����
C��Fe2+����SO4��������Ӧ�����IJ���SO4�� �� ����c��Fe2+������ʱ��4��CP�����ʷ����½�����C����
D�����ɵ�Fe3+ˮ��ʹ��Һ��������ǿ�������������4��CP�Ľ��⣬��D����
��ѡAC��
�۵�c��Fe2+��=3.2��10��3molL��1ʱ��4��CP������Ϊ52.4%��4��CP�����ƽ����Ӧ���ʵļ������ʽΪ ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ��
��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ������������������֯��������������������е��ܼ���ʯ�ͺ�ҽҩ��ҵ�е���ȡ����Ҳ�������ϸ����Լ��㽶�����ܡ��ӡ���ȶ�����ζ���ijɷ֣�ʵ�����Ʊ������������Ļ�ѧ����ʽΪ��CH3COOH+CH3CH2CH2CH20H ![]() CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
�Ʊ������л������еĸ���Ӧ��
2CH3CH2CH2CH2OH ![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O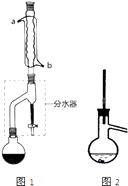
��Ҫʵ�鲽�����£�
��ϳɣ�
�ڸ����Բ����ƿ�м�11.5mL��9.3g��0.125mol����������7.2mL��7.5g��0.125mol���������3��4��ŨH2SO4 �� ҡ�ȺӼ�����ʯ���ٰ�ͼ1ʾװ�ð�װ�ã��ڷ�ˮ����Ԥ�ȼ���5.00mLˮ����ˮ����ڷ�ˮ������֧������3��5mm��Ȼ����С����ȣ���Ӧ��Լ40min��
��������ᴿ��
�ٽ���ƿ�з�Ӧ��Ļ������ȴ�����ˮ���е�����ϲ���ת���Һ©����������10mLˮ��10mL 10%̼������Һϴ�������ԣ�pH=7����������ã���ȥˮ�㣮
�ڽ����㵹��С��ƿ�У���������ˮ����þ���
�۽������������ֲ�Ʒת��50mL������ƿ�У��Ӽ�����ʯ���г�ѹ�����ռ���Ʒ����Ҫ�Լ�������������������£�
������ | ������ | ������ | ���������� | ������ |
�ܶ�/gmL��1 | 0.810 | 1.049 | 0.882 | 0.7689 |
�е�/�� | 117.8 | 118.1 | 126.1 | 143 |
��ˮ�е��ܽ��� | ���� | ���� | ���� | ���� |
����������Ϣ�ش��������⣺
��1����ͼ1����װ�ÿɿ����ɷ�ˮ����Բ����ƿ�������������ƣ���ɣ�������ˮӦ������a��b���ܿ�ͨ�룮
��2������жϸúϳɷ�Ӧ�ﵽ���յ㣺 ��
��3���ڲ��������ʱ��������ѹס��Һ©���IJ�������������ס����Һ©����ת��������������ҡ���κ�Ҫ����������ʱ֧�ܿڲ��ܶ����˺ͻ��ڲ�������ں���������ˮ����þ�����Ӧ������ʵ��������ƣ���Ȼ�������������ֲ�Ʒת��������ƿ�У�
��4������۵ij�ѹ���������һ�����¶ȣ�����Ϊ���м��ȱȽϺ��ʣ��������ѡ����ѡ��A��ˮ B�����ͣ��е�290�棩 C��ɰ�� D��ʯ���ͣ��е�200��300�棩
�������װ����ͼ2��ʾ�����ռ����IJ�Ʒ�п��ܻ������ʣ�
��5����Ӧ���������ų���ˮΪ6.98mL��ˮ���ܶ�Ϊ1gmL��1��������������ת����ԼΪ ��
����Ŀ��ijͬѧ���о�Ԫ�����ʵݱ����ʵ��ʱ���Լ������һ��ʵ�鷽��������¼���й�ʵ������(���±������е���ʵ�鷽��������ʵ��������ǰ��һ���Ƕ�Ӧ��ϵ)��
ʵ�鲽�� | ʵ������ |
����þ����ɰֽ��ĥ�����Թ��У���������ˮ������ˮ���ڣ�������Һ�еμӷ�̪��Һ | A.����ˮ���ϣ��۳�С���Ĵ��ζ���������˻˻��������֮��ʧ����Һ��ɺ�ɫ |
�������Ƶ�Na2S��Һ�еμ����Ƶ���ˮ | B.�������������Һ���dz��ɫ |
����һС������Ʒ�����з�̪��Һ����ˮ�� | C.���ҷ�Ӧ��Ѹ�ٲ���������ɫ���� |
����þ��Ͷ��ϡ������ | D.��Ӧ��ʮ�־��ң�������ɫ���� |
��������Ͷ��ϡ������ | E.���ɰ�ɫ��״�������̶�������ʧ |
����AlCl3��Һ�еμ�NaOH��Һ������ | F.���ɵ���ɫ���� |
���������ͬѧ���������ʵ�鱨�档
��1��ʵ��Ŀ�ģ��о�__________________Ԫ�����ʵݱ���ɡ�
��2��ʵ����Ʒ���Լ��������ơ�þ����������ϡ���ᡢ������ˮ������Na2S��Һ��AlCl3��Һ��NaOH��Һ����̪��Һ�ȡ�
������________��________����ֽ���ԹܼС���ͷ�ιܡ����ӡ��ձ���С��������Ƭ��ɰֽ�����ȡ�
��3��ʵ�����ݣ�(��д��ʵ�鲽���Ӧ��ʵ������ı�ź��٢��Ļ�ѧ����ʽ����ʵ��Ľ���)
ʵ������ | �� | �� | �� | �� | �� | �� |
ʵ������(��A��F) | ____ | ____ | __ | ____ | ____ | ____ |
��_________________________________________________��
��_____________________________________________��
��ʵ��Ľ��ۣ�________________________________________________________________��