题目内容
下列方程式书写正确的是
A 、H2SO3的电离方程式H2SO3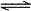 2H++SO32-
2H++SO32-
B、HCO3-在水溶液中的电离方程式:HCO3-+H2O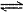 H3O++CO32-
H3O++CO32-
C、CO32-的水解方程式:CO32-+2H2O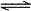 H2CO3+2OH-
H2CO3+2OH-
D、CaCO3的电离方程式:CaCO3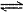 Ca2++CO32-
Ca2++CO32-
A 、H2SO3的电离方程式H2SO3
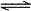 2H++SO32-
2H++SO32-B、HCO3-在水溶液中的电离方程式:HCO3-+H2O
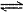 H3O++CO32-
H3O++CO32- C、CO32-的水解方程式:CO32-+2H2O
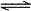 H2CO3+2OH-
H2CO3+2OH-D、CaCO3的电离方程式:CaCO3
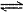 Ca2++CO32-
Ca2++CO32-B
试题分析:A不正确,亚硫酸是弱酸,电离是分步的;C不正确,CO32-的水解也是分步进行的;D不正确,碳酸钙是强电解质,用等号连接,答案选B。
点评:盐类水解大部分都是可逆的,因此用可逆号连接。多元弱酸跟离子是分步水解的,而多元弱碱的阳离子水解是一步到位的。同样弱电解质的电离是可逆的,也用可逆号连接。其中多元弱酸的电离也是分步的,多元弱碱的电离是一步到位的,而强电解质的电离是完全电离的,用等号连接。

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
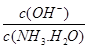 增大
增大