题目内容
【题目】下列离子方程式书写正确的是
A.碳酸钠溶液中逐滴加入等物质的量的乙酸 CO32-+2CH3COOH=CO2↑+H2O+2CH3COO-
B.二氧化硫通入NaClO溶液中:SO2+H2O+2ClO-=SO32-+2HClO
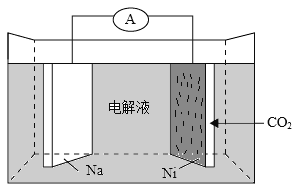
C.用碳棒作电极电解氯化钠饱和溶液 2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
D.碳酸钡溶于氢氟酸 BaCO3+2H+=Ba2++H2O+CO2↑
【答案】C
【解析】
A. 碳酸钠溶液中逐滴加入等物质的量的乙酸 ,碳酸根与醋酸之比为1:1,则方程式为CO32-+CH3COOH= HCO3-+CH3COO-,故A错误;
B. 次氯酸根具有强氧化性,二氧化硫有还原性,故反应产物应为氯离子和硫酸根离子,故B错误;
C. 用碳棒作电极电解氯化钠饱和溶液 2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑,C正确;
2OH-+H2↑+Cl2↑,C正确;
D. HF为弱电解质,在离子方程式中不拆,故D错误;
故答案选C。

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
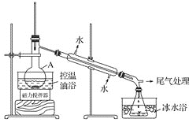
黄冈天天练口算题卡系列答案【题目】溴主要以Br- 形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程示意如下。
![]()
资料:常温下溴呈液态,深红棕色,易挥发。
(1)酸化:将海水酸化的主要目的是避免_______(写离子反应方程式)。
(2)脱氯:除去含溴蒸气中残留的Cl2
①具有脱氯作用的离子是_______。
②溶液失去脱氯作用后,补加FeBr2或加入_______,脱氯作用恢复。
(3)富集、制取Br2:
用Na2CO3溶液吸收溴,Br2歧化为BrO3- 和Br-。再用H2SO4酸化歧化后的溶液得到Br2,其离子反应方程式为_______。
(4)探究(3)中所用H2SO4浓度对Br2生成的影响,实验如下:
序号 | A | B | C |
试剂组成 | 1 mol/L NaBr 20% H2SO4 | 1 mol/L NaBr 98% H2SO4 | 将B中反应后溶液用水稀释 |
实验现象 | 无明显现象 | 溶液呈棕红色,放热 | 溶液颜色变得很浅 |
①B中溶液呈棕红色说明产生了_______。
②分析C中溶液颜色变浅的原因,甲同学认为是发生了化学反应所致;乙同学认为是用水稀释所致。若认为甲同学的分析合理,请用具体的反应说明理由;若认为乙同学的分析合理,进一步设计实验方案说明。理由或方案:_______。
③酸化歧化后的溶液宜选用的酸是______(填“稀硫酸”或“浓硫酸”)。