题目内容
实验室通常悬挂涂有CuI的滤纸监测空气中汞蒸气的含量.反应方程式为:4CuI+Hg═Cu2HgI4+2Cu,下列叙述正确的是( )
| A、4mol CuI反应后得到2mol电子 |
| B、4mol CuI反应后失去4mol电子 |
| C、lmol Hg反应后得到2mol电子 |
| D、1mol Hg反应后失去4mol电子 |
考点:氧化还原反应的电子转移数目计算
专题:氧化还原反应专题
分析:反应4CuI+Hg═Cu2HgI4+2Cu中,Cu元素化合价部分由+1价降低到0价,被还原,CuI为氧化剂,Hg元素化合价由0价升高到+2价,Hg为还原剂,结合元素化合价的变化解答该题.
解答:
解:A.Cu元素化合价部分由+1价降低到0价,降低1,当有4molCuI参加反应,只有2molCu元素的化合价发生变化,故转移2mol电子,故A正确;
B.当有4molCuI参加反应,只有2molCu元素的化合价发生变化,转移2mol电子,故B错误;
C.Hg元素化合价部分由0价升高到+2价,升高2,失去2个电子,故当有1molHg参加反应,失去2mol电子,故C错误;
D.1molHg参加反应,失去2mol电子,故D错误,
故选:A.
B.当有4molCuI参加反应,只有2molCu元素的化合价发生变化,转移2mol电子,故B错误;
C.Hg元素化合价部分由0价升高到+2价,升高2,失去2个电子,故当有1molHg参加反应,失去2mol电子,故C错误;
D.1molHg参加反应,失去2mol电子,故D错误,
故选:A.
点评:本题考查氧化还原反应,难度不大,注意从元素化合价的角度分析得失电子的情况和数目.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入足量CO2.
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入足量CO2.
| A、只有②③④⑤ | B、只有①②⑤ |
| C、只有②③⑤ | D、全部 |
有关钠的叙述不正确的是( )
| A、少量钠应保存在煤油中,实验后剩余的钠需放回原瓶 |
| B、2.3g钠与97.7g水反应后溶液中溶质的质量分数大于4% |
| C、钠与CuSO4溶液反应生成的蓝色沉淀上有时出现暗斑,这是析出的金属铜 |
| D、用一般的化学还原法不能制取金属钠,但可用电解熔化NaCl的方法制得 |
下列物质中,互为同分异构体的是( )
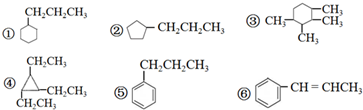

| A、①② | B、①⑤ | C、①④ | D、①③④ |
今年全国低碳日活动的主题是:“携手节能低碳、共建碧水蓝天”.下列措施与这主题不相符的是( )
A、 焚烧废弃塑料 |
B、 处理污水 |
C、 风力发电 |
D、 推广电动汽车 |
下列数据是对应物质的熔点,有关的判断错误的是( )
| Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 |
| 920℃ | 97.8℃ | 1291℃ | 190℃ | 2073℃ | -107℃ | -57℃ | 1723℃ |
| A、含有金属阳离子的晶体不一定是离子晶体 |
| B、在共价化合物分子中各原子都形成8电子结构 |
| C、同族元素的氧化物可形成不同类型的晶体 |
| D、金属晶体的熔点不一定比分子晶体的高 |
下列说法正确的是( )
| A、在“食醋总酸含量的测定”实验中,选择酚酞溶液为指示剂,当溶液的颜色变为粉红色且在半分钟内不褪色,即达到滴定终点 |
| B、在“牙膏中某些主要成分的检验”实验中,在牙膏与蒸馏水搅拌、静置分离后的澄清溶液中加入少量的新制Cu(OH)2,当产生绛蓝色沉淀时,说明牙膏中含有甘油 |
| C、在“阿司匹林的合成”实验中,把从盐酸中析出的晶体进行抽滤,用酒精洗涤晶体1~2次,然后抽滤,将晶体转移到表面皿上,干燥后称其质量,计算产率 |
| D、人体吸入氯气、氯化氢气体时,可吸入少量酒精或乙醚的混合蒸气解毒;氨气、溴中毒休克时要马上进行人工呼吸 |