题目内容
I,已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数分别为:
醋酸K =1.75×10-5
碳酸K1=4. 30×10-7 K2=5.61×10-11
亚硫酸K1=1.54×10-2 K2=1.02×10-2
(1)写出碳酸的第一级电离平衡常数的表达式:K1=___。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱:____>____>___ 。
(3)若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是___(填序号)。
A.c(CH3COO -)
B.c(H+)
C.醋酸电离平衡常数
D.醋酸的电离程度
Ⅱ,某化工,一废水中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01 mol.L-1。排放前拟用沉淀法除去这两种离子,查找有关数据如下:
醋酸K =1.75×10-5
碳酸K1=4. 30×10-7 K2=5.61×10-11
亚硫酸K1=1.54×10-2 K2=1.02×10-2
(1)写出碳酸的第一级电离平衡常数的表达式:K1=___。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱:____>____>___ 。
(3)若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是___(填序号)。
A.c(CH3COO -)
B.c(H+)
C.醋酸电离平衡常数
D.醋酸的电离程度
Ⅱ,某化工,一废水中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01 mol.L-1。排放前拟用沉淀法除去这两种离子,查找有关数据如下:

(4)你认为往废水中投入____(填字母序号),沉淀效果最好。
A.NaOH
B.Na2S
C.KI
D.Ca(OH)2
(5)如果用食盐处理只含有重金属Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%(密度约为 1 g.mL-1)。若环境要求排放标准为c(Ag+)低于1.0×10-8 mol.L-1,问该工厂处理后的废水中c(Ag+)= _____[已知:Ksp(AgCl) =1.8×10-10]。
A.NaOH
B.Na2S
C.KI
D.Ca(OH)2
(5)如果用食盐处理只含有重金属Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%(密度约为 1 g.mL-1)。若环境要求排放标准为c(Ag+)低于1.0×10-8 mol.L-1,问该工厂处理后的废水中c(Ag+)= _____[已知:Ksp(AgCl) =1.8×10-10]。
(1)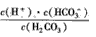
(2)H2CO3 ;HSO3- ;HCO3-
(3)AD
(4)B
(5)9×10 -9 mol . L-1
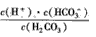
(2)H2CO3 ;HSO3- ;HCO3-
(3)AD
(4)B
(5)9×10 -9 mol . L-1

练习册系列答案
相关题目
I.已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数分别为:
醋酸 K=1.75×10-5
碳酸 K1=4.30×10-7 K2=5.61×10-11
亚硫酸 K1=1.54×10-2 K2=1.02×10-7
(1)写出碳酸的第一级电离平衡常数表达式:K1=______.
(2)在相同条件下,试比较CH3COONa、Na2CO3和Na2SO3水溶液的碱性强弱:______>______>______.
(3)在相同条件下,试比较同浓度同体积H2SO3、NaHSO3和Na2SO3溶液中粒子的数目:______>______>______.
(4)若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是______(填序号).
A.c(CH3COO-) B.c(H+) C.醋酸电离平衡常数 D.醋酸的电离程度
II.某化工厂废水中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(5)你认为往废水中投入______(填字母序号),沉淀效果最好.
A.NaOH B.Na2S C. KI D.Ca(OH)2
(6)如果用食盐处理其只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%.若环境要求排放标准为c(Ag+)低于1.0×10-8mol?L-1,问该工厂处理后的废水中c(Ag+)=______[已知:Ksp(AgCl)=c(Ag+)?c(Cl-)=1.8×10-10mol2?L-2].
醋酸 K=1.75×10-5
碳酸 K1=4.30×10-7 K2=5.61×10-11
亚硫酸 K1=1.54×10-2 K2=1.02×10-7
(1)写出碳酸的第一级电离平衡常数表达式:K1=______.
(2)在相同条件下,试比较CH3COONa、Na2CO3和Na2SO3水溶液的碱性强弱:______>______>______.
(3)在相同条件下,试比较同浓度同体积H2SO3、NaHSO3和Na2SO3溶液中粒子的数目:______>______>______.
(4)若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是______(填序号).
A.c(CH3COO-) B.c(H+) C.醋酸电离平衡常数 D.醋酸的电离程度
II.某化工厂废水中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| KSP | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C. KI D.Ca(OH)2
(6)如果用食盐处理其只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%.若环境要求排放标准为c(Ag+)低于1.0×10-8mol?L-1,问该工厂处理后的废水中c(Ag+)=______[已知:Ksp(AgCl)=c(Ag+)?c(Cl-)=1.8×10-10mol2?L-2].
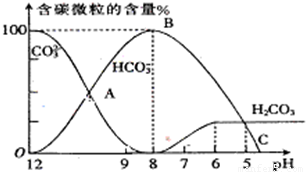
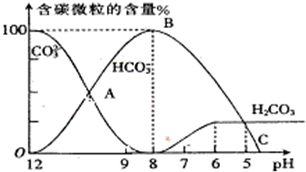 I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题: H++HA- HA-
H++HA- HA- H++A2-
H++A2-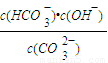 =2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.
=2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______. H++HA- HA-
H++HA- HA- H++A2-
H++A2-