题目内容
【题目】氯化铵俗称卤砂,主要用于干电池、化肥等。某化学研究小组设计如下实验制备卤砂并进行元素测定。
I.实验室用NH3和HCl气体在A中制备卤砂,所需装置如下。
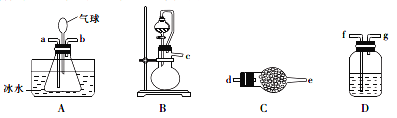
(1)装置接口连接顺序是____________→a; ___________→b。(装置可重复选用)
(2)C装置的作用是__________________,D装置盛装的物质是__________________。
(3)写出用上述装置制备氨气的一组试剂:_____________________。
II.测定卤砂中Cl元素和N元素的质量之比。
该研究小组准确称取ag卤砂,与足量氧化铜混合加热,充分反应后把气体产物按下图装置进行实验。收集装置收集到的气体为空气中含量最多的气体,其体积换算成标准状况下的体积为VL,碱石灰增重bg。
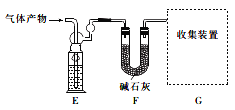
(4)E装置内的试剂为__________,卤砂与氧化铜混合加热反应的化学方程式为_______________。
(5)卤砂中Cl元素和N元素的质量之比为__________________(用含b、v的式子表示)。
(6)为了测定卤砂中氯元素的质量,他们设计的实验方案是将ag卤砂完全溶解于水,加入过量AgNO3溶液,然后测定生成沉淀的质量。请你评价该方案是否合理,并说明理由_______________________。
【答案】c→f→g c→d→e 干燥氨气 浓硫酸 浓氨水和碱石灰(或其他合理答案) 浓硫酸 2NH4Cl+3CuO![]() 3Cu+N2↑+2HCl↑+3H2O
3Cu+N2↑+2HCl↑+3H2O ![]() (或
(或![]() 等其他合理答案) 合理,氯化铵纯净,其电离出的氯离子全部沉淀,故通过沉淀质量可求得氯离子质量(或不合理,氯化铵不纯,杂质离子也发生了沉淀反应等其他合理答案)
等其他合理答案) 合理,氯化铵纯净,其电离出的氯离子全部沉淀,故通过沉淀质量可求得氯离子质量(或不合理,氯化铵不纯,杂质离子也发生了沉淀反应等其他合理答案)
【解析】
I.(1)制取氯化铵,可以由氨气和氯化氢反应制备,应该选用B装置分别制备氨气和氯化氢,干燥除杂后通入A中反应,根据氨气的密度小于氯化氢,应该由b口通入氨气,a口通入氯化氢,因此装置接口连接顺序是c→f→g →a;b←e←d←c,
(2) 根据上述分析,C装置中装入碱石灰可以干燥氨气,D装置盛装浓硫酸可以干燥氯化氢;
(3)根据装置图,可以选用浓氨水和碱石灰制备氨气;
Ⅱ.(4)氯化铵与氧化铜混合加热,发生的反应为2NH4Cl+3CuO![]() 3Cu+N2↑+2HCl↑+3H2O,F装置中的碱石灰可以吸收氯化氢,则E装置内可以装入浓硫酸,吸收反应过程中生成的水蒸气,G装置用于收集氮气;
3Cu+N2↑+2HCl↑+3H2O,F装置中的碱石灰可以吸收氯化氢,则E装置内可以装入浓硫酸,吸收反应过程中生成的水蒸气,G装置用于收集氮气;
(5)氮气的物质的量为![]() =
=![]() mol,氯化氢的物质的量为
mol,氯化氢的物质的量为![]() =
=![]() ,卤砂中Cl元素和N元素的质量之比为
,卤砂中Cl元素和N元素的质量之比为![]() ×35.5g/mol:
×35.5g/mol:![]() mol×28g/mol=
mol×28g/mol=![]() ;
;
(6)若氯化铵纯净,其电离出的氯离子全部沉淀,故通过沉淀质量可求得氯离子质量,因此该方案合理((或不合理,氯化铵不纯,杂质离子也发生了沉淀反应等其他合理答案)。
I.(1)制取氯化铵,可以由氨气和氯化氢反应制备,应该选用B装置分别制备氨气和氯化氢,干燥除杂后通入A中反应,根据氨气的密度小于氯化氢,应该由b口通入氨气,a口通入氯化氢,因此装置接口连接顺序是c→f→g →a;b←e←d←c ,
故答案为:c→f→g; e←d←c;
(2) 根据上述分析,C装置中装入碱石灰可以干燥氨气,D装置盛装浓硫酸可以干燥氯化氢,故答案为:干燥氨气;浓硫酸;
(3)根据装置图,可以选用浓氨水和碱石灰制备氨气,
故答案为:浓氨水和碱石灰(或其他合理答案);
Ⅱ.(4)氯化铵与氧化铜混合加热,发生的反应为2NH4Cl+3CuO![]() 3Cu+N2↑+2HCl↑+3H2O,F装置中的碱石灰可以吸收氯化氢,则E装置内可以装入浓硫酸,吸收反应过程中生成的水蒸气,G装置用于收集氮气;
3Cu+N2↑+2HCl↑+3H2O,F装置中的碱石灰可以吸收氯化氢,则E装置内可以装入浓硫酸,吸收反应过程中生成的水蒸气,G装置用于收集氮气;
故答案为:浓硫酸;2NH4Cl+3CuO![]() 3Cu+N2↑+2HCl↑+3H2O;
3Cu+N2↑+2HCl↑+3H2O;
(5)氮气的物质的量为![]() =
=![]() mol,氯化氢的物质的量为
mol,氯化氢的物质的量为![]() =
=![]() ,卤砂中Cl元素和N元素的质量之比为
,卤砂中Cl元素和N元素的质量之比为![]() ×35.5g/mol:
×35.5g/mol:![]() mol×28g/mol=
mol×28g/mol=![]() =
=![]() ;
;
故答案为:![]() (或
(或![]() );
);
(6)若氯化铵纯净,其电离出的氯离子全部沉淀,故通过沉淀质量可求得氯离子质量,因此该方案合理((或不合理,氯化铵不纯,杂质离子也发生了沉淀反应等其他合理答案)。
故答案为:合理,氯化铵纯净,其电离出的氯离子全部沉淀,故通过沉淀质量可求得氯离子质量(或不合理,氯化铵不纯,杂质离子也发生了沉淀反应等其他合理答案)。

 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案【题目】以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)CO(g)+H2(g)△H=+131.3kJmol﹣1
①该反应在常温下_______自发进行(填“能”与“不能”);
②一定温度和压强下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是__________(填字母,下同)
a.容器中的压强不变
b.1mol H﹣H键断裂的同时断裂2mol H﹣O
c.c(CO)=c(H2)
d.密闭容器的容积不再改变
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)CO2(g)+H2(g),得到如表三组数据:
实验组 | 温度 ℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | H2 | CO | |||
① | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
② | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
③ | 900 | a | b | c | d | t |
①该反应为_________(填“吸”或“放”)热反应;实验②条件下平衡常数K=___________。
②实验①中从反应开始至平衡以CO2表示的平均反应速率为V(CO2)=____________(取小数点后两位)
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:CO2(g)+3H2(g)CH3H(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJmol﹣1)的变化.在体积为1L 的恒容密闭容器中,充入1mol CO2和3mol H2, 下列措施中能使c (CH3OH)增大的是_____________.
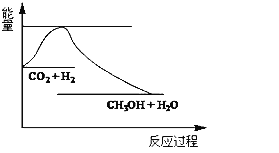
A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来
D.再充入1mol CO2和3mol H2.
【题目】近期我国冀东渤海湾发现储量达10亿吨的大型油田,下列说法正确的是( )
A. 石油属于可再生矿物能源 B. 石油主要含有碳、氢两种元素
C. 石油的裂化是物理变化 D. 石油分馏的各馏分均是纯净物
【题目】钼酸钠晶体(Na2MoO4·2H2O)可抑制金属腐蚀。以钼精矿(主要成分为MoS2,含少量杂质)为原料,制备钼酸钠晶体的主要流程图如下。
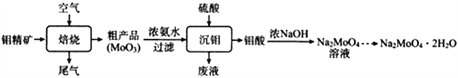
回答下列问题
(1)完成下列反应:_____MoS2+ _____O2![]() _____SO2+ _____MoO3
_____SO2+ _____MoO3
在焙烧炉中,空气从炉底进入矿石经粉碎后从炉顶进入,这样处理的目的是__________________。
(2)浓氨水浸取粗产品获得(NH4)2MoO4溶液,其化学反应方程式为____________________________;该反应说明MoO3______(填“有”或“没有”)酸性氧化物的性质。
(3)常温下,沉钼阶段所得废液为(NH4)2SO4稀溶液。若(NH4)2SO4稀溶液的pH=a,则![]() =_______(用含a的代数式表示,NH3·H2O的Kb=1.8×10-5),若将此稀溶液蒸发浓缩,
=_______(用含a的代数式表示,NH3·H2O的Kb=1.8×10-5),若将此稀溶液蒸发浓缩,![]() 将_________(填“变大”“不变”或“变小”)。
将_________(填“变大”“不变”或“变小”)。
(4)已知钼酸钠在一定温度范围内的析出物质及相应物质的溶解度如下表所示,获得Na2MoO4·2H2O的操作为_____________。
温度(℃) | 0 | 4 | 9 | 10 | 15.5 | 32 | 51.5 | 100 |
析出物质 | Na2MoO4·10H2O | Na2MoO4·2H2O | ||||||
溶解度 | 30.63 | 33.85 | 38.16 | 39.28 | 39.27 | 39.82 | 41.27 | 45. |
结晶得到的母液可以在下次结晶时重复使用,但达到一定次数后必须净化处理,原因是_____________。
(5)空气中钼酸盐对碳钢的缓蚀原理是在钢铁表面形成FeMoO4-Fe2O3保护膜,在密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入钼酸盐外还需加入的物质是___________(填选项字母)。
A. NaNO2 B.通入适量N2 C.油脂 D.盐酸


