题目内容
14.下列各组有机物,只用溴水就能鉴别的是( )| A. | 己烯 苯 四氯化碳 | B. | 苯 己烯 己炔 | ||
| C. | 苯 己烷 己炔 | D. | 溴己烷 苯 己烯 |
分析 含有不饱和键的物质能与溴水发生加成反应而使溴水褪色,结合有机物的水溶性以及密度进行鉴别.
解答 解:A.己烯含有C=C键,可与溴水发生加成反应而使溴水褪色,苯和四氯化碳与溴水都不反应,但苯的密度不水小,色层在上层,四氯化碳的密度比水大,色层在下层,可鉴别,故A正确;
B.己炔、己烯都为不饱和烃,都能与溴水反应,不能鉴别,故B错误;
C.苯、己烷都不与溴反应,且密度比水小,无法鉴别,故C错误;
D.溴己烷密度比水大,加入溴色层在下层,苯的密度比水小,加入溴水色层在上层,己烯可与溴发生加成反应,溴水褪色,可鉴别,故D正确.
故选AD.
点评 本题考查有机物的鉴别,为高频考点,侧重于学生的分析能力和实验能力的考查,题目难度不大,注意把握常见有机物的性质,特别是水溶性和密度.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列有机物命名正确的是( )
| A. | 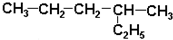 2-乙基戊烷 2-乙基戊烷 | B. | 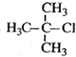 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | ||
| C. | 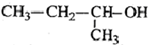 2-甲基-1-丙醇 2-甲基-1-丙醇 | D. |  2-甲基-3-丁炔 2-甲基-3-丁炔 |
5.一定温度下反应2SO2(g)+O2(g)?2SO3(g)达到化学平衡状态的标志是( )
| A. | SO2,O2和SO3的体积分数不再改变 | |
| B. | c(SO2):c(O2):c(SO3)=2:1:2 | |
| C. | SO2与O2的物质的量之和是SO3的物质的量2倍 | |
| D. | 单位时间里每增加2molSO2,同时增加1molO2 |
2.在中和热的实验测定中,下列操作中使结果偏高的是( )
| A. | 实验装置保温、隔热效果差 | |
| B. | 量取酸碱溶液的体积时仰视读数 | |
| C. | 分多次把NaOH溶液倒入盛有硫酸的小烧杯中 | |
| D. | 用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 |
9.下列物质与水混合后静置,不出现分层的是( )
| A. | 苯 | B. | 三氯甲烷 | C. | 乙酸 | D. | 四氯化碳 |
19.福岛核电站泄漏的放射性物质中含有${\;}_{53}^{131}$I,下列有关${\;}_{53}^{131}$I的说法正确的是( )
| A. | 由此可确定碘元素的相对原子质量为131 | |
| B. | ${\;}_{53}^{131}$I是碘元素的一种核素 | |
| C. | ${\;}_{53}^{131}$I核素中含中子数为53 | |
| D. | ${\;}_{53}^{131}$I2的摩尔质量为262g |
3.已知分解1mol H2O2放出热量98KJ.在含有少量I-的溶液中,H2O2分解的机理为:①H2O2+I-=H2O+IO-(慢)②H2O2+IO-=H2O+O2+I-(快)下列有关该反应的说法正确的是( )
| A. | 反应速率与I-浓度有关 | B. | IO-也是该反应的催化剂 | ||
| C. | 该化学反应速率由反应②决定 | D. | v(H2O2)=v(H2O)=v(O2) |
4.下列各组元素最高价氧化物对应水化物碱性渐弱,酸性渐强的是( )
| A. | NaOH、Mg(OH)2、H3PO4、H2SO4 | B. | NaOH、KOH、H2SO4、HClO4 | ||
| C. | Be(OH)2、Ca(OH)2、HBrO4、HClO4 | D. | Mg(OH)2、Ba(OH)2、H3PO4、H2SO4 |