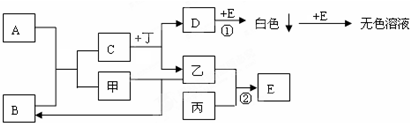
题目内容
17.运用元素周期表的变化规律,推断下列说法不正确的是( )| A. | 铍是一种轻金属,它的氧化物对应水化物可能是两性 | |
| B. | 砹是一种有色固体,它的气态氢化物很不稳定,砹化银是有色不溶于稀HNO3的沉淀 | |
| C. | 硫酸锶难溶于水和稀HNO3,其氢氧化物为强碱 | |
| D. | 硒化氢是无色无味气体,没有H2S稳定 |
分析 A.元素周期表中的对角线规则,处于对角线的元素具有相似性;
B.根据卤素单质颜色、状态变化,推测砹是一种有色固体,元素的非金属性越弱,其氢化物越不稳定,根据AgCl、AgBr、AgI颜色及溶解性判断;
C.同主族元素及其化合物的性质具有相似性,金属性越强,最高价氧化物对应水化物的碱性越强;
D.由水、硫化氢气味变化,可知硒化氢可能为有味气体,元素的非金属性越弱,其氢化物越不稳定.
解答 解:A.元素周期表中Be和Al处于对角线位置上,处于对角线的元素具有相似性,Be、BeO、Be(OH)2均有两性,故A正确;
B.卤族元素性质具有相似性,自上而下颜色加深、物质熔点升高,元素非金属性减弱,氢化物稳定性减弱,AgCl、AgBr、AgI颜色依次加深均难溶于硝酸,可推知砹(At)为有色固体,HAt不稳定,AgAt是不溶于硝酸的有色固体,故B正确;
C.锶与钡是同主族元素,BaSO4是难溶于水和盐酸的白色固体,所以SrSO4也是难溶于水和硝酸的白色固体,锶的金属性强于钡,故氢氧化锶属于强碱,故C正确;
D.元素的非金属性越弱,其氢化物越不稳定,Se的非金属性小于S,则硒化氢(H2Se)不如H2S稳定,由水、硫化氢气味变化,可知硒化氢可能为有味气体,故D错误;
故选D.
点评 本题考查元素周期律知识,侧重于学生分析能力的考查,注意把握元素周期律的递变规律以及元素的性质与对应单质、化合物的性质的关系,难度不大.

练习册系列答案
相关题目
12.下列检验试剂选用正确的是( )
| A. | 用氯水、KSCN溶液检验FeCl3溶液中是否有FeCl2 | |
| B. | 用酸性高锰酸钾溶液检验FeCl3溶液中是否有FeCl2 | |
| C. | 用NaOH溶液检验MgCl2溶液中是否有FeCl2 | |
| D. | 用硝酸检验某黄色固体是黄铜还是纯铜 |
5.能正确表示下列反应的方程式的是( )
| A. | 用铜电极电解饱和氯化钠溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| B. | 过量铁与氯气反应:2Fe+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3 | |
| C. | 过氧化钠与水反应:2O22-+2H2O=4OH-+O2↑ | |
| D. | 向石灰水中滴加少量Ca(HCO3)2溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
2.在100kPa下,12g石墨完全转化为金刚石需要吸收1.895kJ的热能.据此在100kPa时,下列说法正确的是( )
| A. | 石墨转化为金刚石不是化学变化 | |
| B. | 金刚石比石墨稳定 | |
| C. | 1mol石墨具有的总能量比1mol金刚石的低 | |
| D. | 等质量的石墨与金刚石完全燃烧,石墨放出的能量多 |
9.线型弹性材料“丁苯吡橡胶”的结构简式如下:
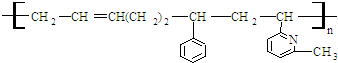
其单体可能是:
① ②CH2=CH
②CH2=CH ③CH2=CH-CH═CH2④CH3-CH═CHH-CH2
③CH2=CH-CH═CH2④CH3-CH═CHH-CH2
⑤CH2═CH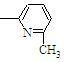 ⑥CH2=CH
⑥CH2=CH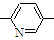 CH3
CH3
正确的组合是( )

其单体可能是:
①
 ②CH2=CH
②CH2=CH ③CH2=CH-CH═CH2④CH3-CH═CHH-CH2
③CH2=CH-CH═CH2④CH3-CH═CHH-CH2
⑤CH2═CH
 ⑥CH2=CH
⑥CH2=CH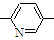 CH3
CH3正确的组合是( )
| A. | ②③⑥ | B. | ②③⑤ | C. | ①②⑥ | D. | ②④⑥ |
7.通过下列方法,不可能将分子式为C2H6O的有机物的同分异构体,区别开来的是( )
| A. | 红外光谱 | B. | 核磁共振氢谱 | C. | 燃烧法 | D. | 与钠反应 |
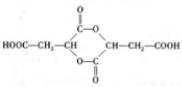 ;
;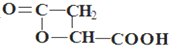 .
.