题目内容
(1)X原子在第二电子层上只有一个空轨道,则X是 (填元素符号,下同);其电子排布图为 ;
(2)R原子的3p轨道上只有一个未成对电子,则R原子可能是 、 ;
(3)Y原子的核电荷数为29,其外围电子排布式是 ,其在元素周期表中的位置是 .
(2)R原子的3p轨道上只有一个未成对电子,则R原子可能是
(3)Y原子的核电荷数为29,其外围电子排布式是
考点:原子核外电子排布
专题:
分析:(1)X原子在第二电子层上只有一个空轨道,则价层电子排布式为2s22p2,则X是C元素,根据构造原理书写其核外电子排布式;
(2)R原子的3p轨道上只有一个未成对电子,则R原子3p轨道上可能含有1个电子或5个电子,据此判断R元素;
(3)Y原子的核电荷数为29,则Y是Cu元素,其3d、4s电子为其外围电子,根据能量最低原理书写其外围电子排布式,根据元素的电子层数与其周期数相等根据最后排入的电子判断该元素在元素周期表中的位置;
(2)R原子的3p轨道上只有一个未成对电子,则R原子3p轨道上可能含有1个电子或5个电子,据此判断R元素;
(3)Y原子的核电荷数为29,则Y是Cu元素,其3d、4s电子为其外围电子,根据能量最低原理书写其外围电子排布式,根据元素的电子层数与其周期数相等根据最后排入的电子判断该元素在元素周期表中的位置;
解答:
解:(1)X原子在第二层上只有一个空轨道,则L层的2p能级含有一个空轨道,则X核外电子数是6,为C元素,其核外电子排布式为:1S22S22P2;
故答案为:C;1S22S22P2;
(2)R原子的3p轨道上只有一个未成对电子,则价层电子排布式为3s23p1或3s23p5,则R为Al元素或Cl元素,
故答案为:Al或Cl;
(3)Y原子的核电荷数为29,为Cu元素,核外电子排布式为1s22s22p63s23p63d104s1,其外围电子排布式是3d104s1,处于周期表中第四周期第ⅠB族,
故答案为:3d104s1;第四周期第ⅠB族;
故答案为:C;1S22S22P2;
(2)R原子的3p轨道上只有一个未成对电子,则价层电子排布式为3s23p1或3s23p5,则R为Al元素或Cl元素,
故答案为:Al或Cl;
(3)Y原子的核电荷数为29,为Cu元素,核外电子排布式为1s22s22p63s23p63d104s1,其外围电子排布式是3d104s1,处于周期表中第四周期第ⅠB族,
故答案为:3d104s1;第四周期第ⅠB族;
点评:本题考查了原子核外电子排布,明确原子结构、元素周期表结构再结合构造原理来分析解答,知道元素周期表所属区域、元素在周期表中的位置等知识点是解本题关键,题目难度中等.

练习册系列答案
相关题目
下列粒子(或化学键)的数目之比不是1:1的是( )
| A、氘原子中的质子和中子 |
| B、Na2O2固体中的阴离子和阳离子 |
| C、CO2分子中的σ键和π键 |
| D、常温下,pH=7的CH3COOH与CH3COONa混合溶液中的H+与OH- |
下面关于实验操作、现象或原理的叙述中正确的是( )
| A、在“阿司匹林的合成”实验中,把从盐酸中析出的晶体进行抽滤,用乙醇洗涤晶体1~2次,然后抽滤,将晶体转移到表面皿上,干燥后称其质量,计算产率 |
| B、晶体颗粒的大小与结晶条件有关,溶质的溶解度越小,或溶液的浓度越高,或溶剂的蒸发速度越快,析出的晶粒就越细小 |
| C、牙膏中的保湿剂(甘油),可用氢氧化铜浊液根据产生的绛蓝色沉淀来检验 |
| D、在试管中将一定量的浓硝酸、浓硫酸和苯混合,用酒精灯直接加热几分钟,即可制得硝基苯 |
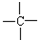 和
和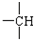 等结合成的.如果某烷分子中同时存在这4种基团,所含碳原子数最小,这种烷烃分子应含
等结合成的.如果某烷分子中同时存在这4种基团,所含碳原子数最小,这种烷烃分子应含