题目内容
下列各装置中都盛有0.1 mol·L-1的NaCl溶液,放置相同时间后,锌片的腐蚀速率由快到慢的顺序是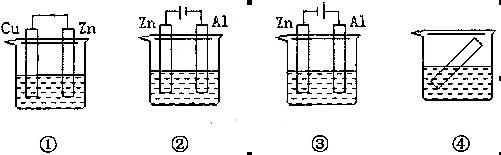
| A.③①④② | B.①②④③ | C.②①④③ | D.②①③④ |
C
解析试题分析:锌片的腐蚀速率由快到慢的顺序是电解池(锌片做正极)>原电池(锌片做负极)>普通金属腐蚀>被保护的(金属做原电池正极)>(金属做电解池阴极),所以答案:②①④③。
考点:金属腐蚀速率的快慢

练习册系列答案
相关题目
在电解水制取H2和O2时,为了增强导电性常常要加入一些电解质,最好选用
| A.NaOH | B.HCl | C.NaCl | D.CuSO4 |
如图为一原电池的结构示意图,下列说法中,不正确的是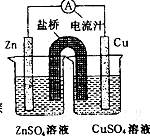
| A.原电池工作时的总反应为Zn+Cu2+=Zn2++Cu |
| B.原电池工作时,Zn电极流出电子,发生氧化反应 |
| C.原电池工作时,铜电极上发生氧化反应,CuSO4溶液蓝色变深 |
| D.盐桥中阳离子流向CuSO4溶液中 |
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电电解一段时间。假设在电解过程中产生的气体全部逸出,下列说法正确的是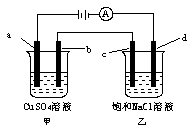
| A.甲、乙两烧杯中溶液的pH均保持不变 |
| B.甲烧杯中a电极反应式为:4OH――4e-=O2↑+2H2O |
| C.当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 |
| D.当b极增重3.2 g时,d极产生的气体为0.56 L(标准状况) |
优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为:2Li+P2VP·nI2 = P2VP·(n-1)I2 +2LiI,则下列说法正确的( )
| A.该电池的电势低,使用寿命比较短 |
| B.电池工作时,碘离子移向P2VP一极 |
| C.聚2-乙烯吡啶的复合物与有机物性质相似,因此不会导电 |
| D.正极的反应为:P2VP·nI2 + 2Li+ + 2e- = P2VP·(n-1)I2 + 2LiI |
下列物质的有关事实与电化学腐蚀无关的是
| A.轮船水线以下的船壳上镶嵌有一定量的锌块 |
| B.镀锌的铁制品比镀锡的铁制品耐用 |
| C.埋在潮湿疏松土壤里的铁管比干燥致密不透气的土壤里的铁管更易被腐蚀 |
| D.在空气中,金属镁、铝的表面可形成一层氧化膜 |
NOx是汽车尾气中的主要污染物之一。通过NOx传感器可监测NOx的含量,其工作原理示意图如下。下列说法正确的是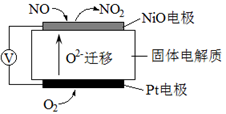
| A.Pt电极作负极,NiO电极作正极 |
| B.Pt电极上发生的是氧化反应 |
| C.NiO电极上发生的是还原反应 |
| D.NiO电极的电极反应式为NO+O2–-2e–=NO2 |
pH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH > a,则该电解质可能是
| A.NaOH | B.H2SO4 | C.AgNO3 | D.Na2SO4 |
图中乙是甲的电解池进行电解时的某个量(纵坐标x)随时间变化的曲线(各电解池都用石墨作电极,不考虑电解过程中溶液浓度变化对电极反应的影响),则x表示( )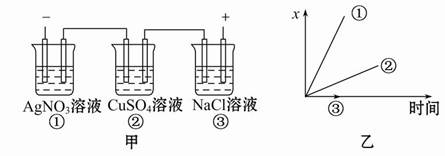
| A.各电解池析出气体体积总数的变化 |
| B.各电解池阳极质量的增加 |
| C.各电解池阴极质量的增加 |
| D.各电极上放电的离子总数的变化 |